已知五种短周期元素的原子半径及主要化合价如下表:
| 元素代号 |
L |
M |
Q |
R |
T |
| 原子半径/nm |
0.160 |
0.143 |
0.104 |
0.111 |
0.066 |
| 主要化合价 |
+2 |
+3 |
+6、-2 |
+2 |
-2 |
下列叙述正确的是
A.L与Q形成的化合物属于共价化合物
B.L、M的单质与稀盐酸反应速率:M>L
C.T、Q的氢化物常温常压下均为无色气体
D.M的最高价氧化物的水化物具有两性
下列有关物理量相应的单位表达错误的是 ( )
A摩尔质量g/mol B气体摩尔体积L/mol C溶解度g/100g D密度g/cm3
下列实验操作中有错误的是 ( )
| A.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B.萃取时,用酒精萃取碘水中的碘 |
| C.蒸馏时,冷却水应从冷凝管的下口通入,上口流出 |
| D.把几滴FeCl3饱和溶液滴入25mL的沸水中加热至液体呈红褐色,制取Fe(OH)3胶体 |
以下是一些常用的危险品标志,装运乙醇的包装箱应贴的图标是 ( )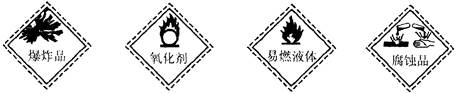
A 爆炸品B 氧化剂C 易燃液体 D 腐蚀品
相同质量的下列脂肪烃,在空气中充分燃烧产生二氧化碳最多的是()
| A.C2H2 | B.C3H6 | C.C4H10 | D.CH4 |
某链状有机物分子中含有n个-CH2-,m个-CH-,a个-CH3,其余为-OH,
则羟基的个数为()
| A.2n+3m-a | B.m+2-a | C.n+m+a | D.m+2n+2-a |