写出下列反应的化学方程式
(1)乙烯和溴的四氯化碳溶液的反应_______________ ___________ 。
(2)乙醇与红热的铜丝反应得到乙醛 。
(3)乙酸乙酯与氢氧化钠反应_________________________________________ 。
卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(1)气态氟化氢中存在二聚分子(HF)2,这是由于。
(2)I3+(可看成II2+)属于多卤素阳离子,根据VSEPR模型推测I3+的空间构型为。
(3)基态溴原子的电子排布式为____________________。碘原子的价电子轨道排布式为_________________。
(4)卤素互化物如BrI、ICl等与卤素单质结构相似、性质相近。Cl2、BrI、ICl沸点由高到低的顺序为________。ICl与水反应的化学方程式为_________。
(5)请推测 ① HClO4、② HIO4、③ H5IO6 [可写成(HO)5IO] 三种物质的酸性由强到弱的顺序为(填序号)。
(6)卤化物RbICl2加热时会分解为晶格能相对较大的卤化物A和卤素互化物或卤素单质,A的化学式为。
CuSO4溶液是中学化学及工农业生产中常见的一种试剂。
(1)某同学配置CuSO4溶液时,向盛有一定量硫酸铜晶体的烧杯中加入适量的蒸馏水,并不断搅拌,结果得到悬浊液。他认为是固体没有完全溶解,于是对悬浊液加热,结果发现浑浊更明显了,原因是,最后,他向烧杯中加入了一定量的溶液,得到了澄清的CuSO4溶液。
(2)该同学利用制得的CuSO4溶液,进行以下实验探究。
① 图一是根据反应Zn + CuSO4 =" Cu" + ZnSO4设计成的锌铜原电池。电解质溶液甲是(填“ZnSO4”或“CuSO4”)溶液;Cu极的电极反应式是。
② 图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是(填“CH4”或“O2”),a处电极上发生的电极反应式是。
(3)将蓝矾、生石灰和水按一定比例混合,即可得到波尔多液(杀菌剂),其有效成分为难溶的碱式硫酸铜[xCuSO4 ·yCu(OH)2]。为测定某碱式硫酸铜的组成进行了如下实验:取等质量的碱式硫酸铜样品两份,一份滴加稀盐酸至恰好完全溶解,另一份高温灼烧后只得到CuO固体。所得数据显示n(HCl)︰n(CuO)=3︰2,则该碱式硫酸铜的化学式中x︰y=。
已知甲、乙、丙、丁、戊为短周期元素形成的五种粒子,它们的电子总数都为18,请回答下列问题:
(1)甲为双核分子,可与水发生置换反应,其化学方程式为____________________;
(2)乙为两种元素形成的双核离子,含该离子的水溶液中加入适量氯水出现浑浊,该反应的离子方程式为________________________________;
(3)丙为含两种元素的分子,且原子个数比为1:1,其水溶液呈弱酸性,写出其主要的电离方程式_______________________________;
(4)丁为六原子分子,若误饮少量丁能使人眼睛失明,则丁中的官能团的电子式为_____________;为了提高一定量的羧酸和丁在一定条件下发生反应时生成物的产率,可采取的措施为____________________;
(5)戊属于烃,与其互为同系物且含五个碳原子的烃的一氯代物共有______种。已知1 g戊在氧气中完全燃烧放出52 kJ的热量,表示2 mol 戊燃烧热的热化学方程式为_________________________________。
经质潜法分析得知,某单烯烃Q的相对分子质量为56;其核磁共振氢谱与红外 光谱表明,Q分子中有两种化学环境不同的氢原子,氢谱峰面积显示两种氢的原子个数比为1∶3。请回答下列问题:
光谱表明,Q分子中有两种化学环境不同的氢原子,氢谱峰面积显示两种氢的原子个数比为1∶3。请回答下列问题:
⑴若Q无顺反异构,则Q的结构简式为。
⑵在锂离子电池中,需要一种有机聚合物作为正负极之问锂离子迁移的介质,该有机聚合物的单体之一(用M表示)的结构简式如下图所示:
M的合成方法之一如下: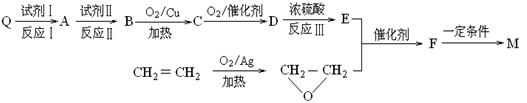
请回答下列问题:
①合成M的反应中,反应I和反应III的反应类型分别是、;
试剂Ⅱ是,C中含有官能团的名称是。
②E的结构简式是。
③M与足量氯氧化钠溶液反应的化学方程式是。
⑶D在一定条件下能发生缩聚反应生成高聚物,请写出D发生缩聚反应的化学方程式。
⑷已知:
若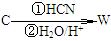 ,请写出符合下列条件的物质的一种结构简式。
,请写出符合下列条件的物质的一种结构简式。
a.碳骨架与W相同;
b.能发生银镜反应;
c.1mol该物质与足量金属钠作用生成1.5molH2;
d.分子中每个碳原子上不同时连有两个官能团。
⑴如图是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。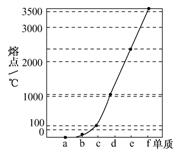
①请写出图中b单质对应元素原子的电子排布式。
②单质a、f对应的元素以原子个数比1∶1形成的分子(相同条件下对H2的相对密度为13)中含个σ键和个π键。
③a与b的元素形成的10电子中性分子X的空间构型为;将X溶于水后的溶液滴入到AgNO3溶液中至过量,得到络离子的化学式为,其中X与Ag+之间以键结合。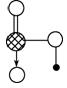
④上图是上述六种元素中的一种元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:。
⑵碳是形成化合物最多的元素,其单质与化合物广布于自然界。
①与碳同周期的非金属元素N的第一电离能大于O的第一电离能,原因是;
②CS2是一种重要的有机溶剂,写出一种与CS2互为等电子体的物质的化学式;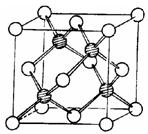
③冰晶胞中水分子的空间排列方式与金刚石晶胞(其晶胞结构如上图,其中空心球所示原子位于立方体的顶点或面心,实心球所示原子位于立方体内)类似。每个冰晶胞平均占有个水分子,冰晶胞与金刚石晶胞微粒排列方式相同的原因是。