铋(Bi)是第VA族元素,+5价Bi的化合物氧化性大于MnO4—。某反应中反应物与生成物有:NaMnO4、NaBiO3、Na2SO4、MnSO4、Bi2(SO4)3、H2O和一种未知物X。下列关于该反应的描述中不正确的是( )
| A.X是H2SO4 |
| B.反应中Mn原子与Bi原子个数比为5:2 |
| C.该反应中NaBiO3作氧化剂 |
| D.该反应中Na2SO4既不是氧化产物,又不是还原产物 |
25℃时,水的电离达到平衡:H2O 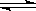 H++OH— ΔH>0,下列叙述正确的是()
H++OH— ΔH>0,下列叙述正确的是()
| A.向水中加入氢氧化钠,平衡逆向移动,c(H+)降低,c(OH―)增大 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw变大 |
| C.向水中加入少量固体CH3COOH,平衡逆向移动,c(H+)降低 |
| D.将水加热,Kw增大,c(H+)不变 |
在一定温度下的恒容容器中,当下列物理量不再发生变化时,表明反应: A(s)+3B(g) 2C(g)+D(g)已达平衡状态的是()
2C(g)+D(g)已达平衡状态的是()
| A.混合气体的压强 | B.混合气体的密度 |
| C.B的生成速率与D的消耗速率之比为3:1 | D.气体的总物质的量 |
等质量的两份锌粉a和b,分别加入过量的稀硫酸中,a中同时加入少量CuSO4溶液,下列各图中表示其产生氢气总体积(V)与时间(t)的关系正确的是 ( )
COCl2(g)  CO(g)+Cl2(g) △H>0。当反应达到平衡时,下列措施:①升温;②恒压通入惰性气体;③增加CO的浓度;④加催化剂;⑤减压;⑥恒容通入惰性气体。能提高COCl2转化率的是
CO(g)+Cl2(g) △H>0。当反应达到平衡时,下列措施:①升温;②恒压通入惰性气体;③增加CO的浓度;④加催化剂;⑤减压;⑥恒容通入惰性气体。能提高COCl2转化率的是
| A.①④⑥ | B.①②⑤ | C.②③⑥ | D.③⑤⑥ |
在25℃时,密闭容器中X、Y、Z三种气体的浓度如下表: 下列说法错误的是()
下列说法错误的是()
| 物质 |
X |
Y |
Z |
| 初始浓度/mol·L-1 |
0.1 |
0.2 |
0 |
| 平衡浓度/mol·L-1 |
0.05 |
0.05 |
0.1 |
 A.反应达到平衡时,X的转化率为50%
A.反应达到平衡时,X的转化率为50% B.改变温度可以改变此反应的平衡常数
B.改变温度可以改变此反应的平衡常数 C.反应可表示为X+3Y
C.反应可表示为X+3Y 2Z,平衡常数为1600
2Z,平衡常数为1600 D.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.增大压强使平衡向生成Z的方向移动,平衡常数增大