2014年“六·五”世界环境日中国主题为“向污染宣战”,旨在体现对治理污染紧迫性和艰巨性的清醒认识,倡导共同行动,努力改善环境,保卫家园。下列说法正确的是
| A.把硝酸工厂的烟囱建造得更高一些,以减少氮氧化物的排放 |
| B.推广燃煤发电,停建核电站,以防核泄漏事故发生 |
| C.将废电池深埋,可以避免其中的重金属污染 |
| D.大量燃烧化石燃料产生的PM2.5是雾霾天气的主要原因之一 |
CH2=CHCOOH不能发生的反应为:
| A.氧化反应 | B.取代反应 | C.加聚反应 | D.水解反应 |
下列变化过程中既破坏了离子键,又破坏了共价键的是:
| A.石油催化裂化 | B.电解无水氯化镁制镁 |
| C.过氧化钠投入水中制氧气 | D.铝与氧化铁发生铝热反应 |
将Xg纯锌粒和Yg锌粉(含银)同时投入足量的等物质的量浓度、等体积的盐酸溶液中(已知:X>Y)。下列叙述正确的为:
| A.开始时的反应速率:V(锌粒)>V(锌粉) |
| B.溶液温度升高的快慢:T(锌粒)>T(锌粉) |
| C.最后放出H2的总量:n(锌粒)>n(锌粉) |
| D.达平衡时正逆反应的速率相等 |
下列说法正确的是:
A.所有有机物都只含C、H、O、N四种元素
B.油脂水解可得到氨基酸和甘油
C.所有烷烃和蛋白质中都存在碳碳单键
D.淀粉和纤维素水解的最终产物都是葡萄糖
对于结构简式如图所示的烃: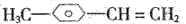 ,下列说法正确的是:
,下列说法正确的是:
| A.分子中一定有9个碳原子处于同一平面 |
| B.分子中只有8个碳原子处于同一平面 |
C.该烃分子式为: |
D.该烃分子式为: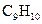 |