要证明溴乙烷中溴的存在,下列各操作步骤:①加入AgNO3溶液;②加入NaOH水溶液;③加热;④加入蒸馏水;⑤加稀硝酸至溶液呈酸性;⑥加入NaOH醇溶液。顺序正确且操作最简单,化学药品选用最少的是( )
| A.④③⑤① | B.②③⑤① | C.④⑥③① | D.⑥③⑤① |
以下关于锂、钠、钾、铷、铯的叙述不正确的是( )
① 氢氧化物中碱性最强的是CsOH② 单质熔点最高的是铯
③ 与O2反应均可得到多种氧化物④ 它们的密度依次增大,均要保存在煤油中
⑤ 其单质的还原性依次增强⑥ 它们对应离子的氧化性依次增强
| A.①③⑤ | B.②④⑥ | C.②③④⑥ | D.①⑤ |
下列判断错误的是()
A.酸性: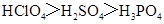 |
B.碱性:NaOH > Mg(OH)2 >Al(OH)3 |
| C.沸点:I2>Br2>Cl2>F2 | D.沸点:HI>HBr>HCl>HF |
若NA表示阿伏加德罗常数的值,下列叙述中正确的是()
| A.7.8 g Na2O2所含离子总数为0.4 NA |
| B.2.0 gD2O(重水)含有的质子数是NA |
| C.标准状况下,0.5 NA个SO3分子所占的体积约为11.2 L |
| D.4℃时,18mL水分子中所含共价键的数目为4 NA |
下列物质中含有共价键的离子化合物是( )
①MgF2②Na2O2③NaOH④NH4Cl⑤CO2⑥H2O2⑦N2
| A.②③④⑤⑦ | B.①②③④⑥ | C.②③④ | D.①③⑤⑥ |
下列物质的化学用语正确的是()
A.溴化钠的电子式: 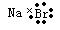 |
B. 14C的原子结构示意图: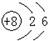 |
| C.HClO的结构式:H-Cl-O | D.原子核内有10个中子的氧原子: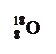 |