在恒温、恒容的密闭容器中反应A(g) B(g)+C(g);△H<0(正反应为放热反应)。若反应物的浓度由2mol/L降到0.8mol/L需20s,那么反应物浓度由0.8mol/L降到0.2mol/L所需的时间为(假设反应温度不变) ( )
B(g)+C(g);△H<0(正反应为放热反应)。若反应物的浓度由2mol/L降到0.8mol/L需20s,那么反应物浓度由0.8mol/L降到0.2mol/L所需的时间为(假设反应温度不变) ( )
| A.10s | B.大于10s | C.小于10s | D.无法判断 |
在一恒定的容器中充入2 mol A和1 mol B发生反应:2A(气)+B(气) x C(气),达到平衡后,C的体积分数为w%;若维持容器的容积和温度不变,按起始物质的量:A为0.6 mol;B为0.3 mol;C为1.4 mol,充入容器,达到平衡后,C的体积分数仍为w%,则x值为()
x C(气),达到平衡后,C的体积分数为w%;若维持容器的容积和温度不变,按起始物质的量:A为0.6 mol;B为0.3 mol;C为1.4 mol,充入容器,达到平衡后,C的体积分数仍为w%,则x值为()
| A.只能为2 | B.可能是2,也可能是3 |
| C.只能为3 | D.无法确定 |
已知NaHSO4在水中的电离方程式为NaHSO4===Na++H++SO42-。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液pH为2。对于该溶液下列叙述中不正确的是()
| A.该温度高于25℃ |
| B.该温度下NaHSO4溶液中,水电离出来的c(H+)=1×10-10mol/L |
| C.该温度下加入等体积pH为12的NaOH溶液可使反应后的溶液恰好呈中性 |
| D.c(H+)=c(OH-)+c(SO42-) |
在密闭容器中发生反应a X(气)+b Y(气) c W(气)+d Z(气),若反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,再次达到平衡时,Z的浓度是原平衡的1.8倍,下列叙述中不正确的是( )
c W(气)+d Z(气),若反应达到平衡后,保持温度不变,将气体压缩到原来的1/2体积,再次达到平衡时,Z的浓度是原平衡的1.8倍,下列叙述中不正确的是( )
| A.平衡向逆反应方向移动 | B.a+b>c+d |
| C.W的体积分数减小 | D.X的转化率降低 |
某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g) 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中再加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是()
3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中再加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是()
| A.m=2 |
| B.两次平衡的平衡常数相同 |
| C.第二次平衡时,Z的浓度为0.4 mol·L-1 |
| D.X与Y的平衡转化率之比为1:1 |
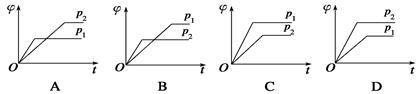
在一定温度、不同压强(p1<p2)下,可逆反应:2X(g) 2Y(s)+Z(g)中,生成物Z在反应混合物中的体积分数(φ)与反应时间(t)的关系有以下图示,其中正确的是 ( )
2Y(s)+Z(g)中,生成物Z在反应混合物中的体积分数(φ)与反应时间(t)的关系有以下图示,其中正确的是 ( )