下列金属中,遇到盐酸或强碱溶液都能放出氢气的是
| A.Cu | B.Mg | C.Fe | D.Al |
黑火药发生爆炸的反应中:S+2KNO3+3C=K2S+N2↑+3CO2↑被还原的元素是
| A.只有N | B.只有S | C.N和S | D.只有C |
短周期主族元素A、B、C、D的原子序数依次增大,A和B形成的气态化合物的水溶液呈碱性,B位于第VA族,A和C同主族,D原子最外层电子数与电子层数相等。下列叙述正确的是
A.原子半径:D>C>B
B.单质的还原性:D>C
C元素A、B、C的氧化物均为非金属氧化物
D.元素B、C、D的最高价氧化物对应的水化物能相互反应
下列结论是从某同学的作业本上摘录的,其中你认为肯定正确的是
①微粒半径:S2->Cl->Cl>S ②氢化物稳定性:HF>HCl>H2S>H2Se
③还原性:S2->Cl->Br->I-④氧化性:Cl2>S>Se
⑤酸性:H2SO4>HClO4>H2SeO4 ⑥得电子能力:F>Cl>Br>I
| A.只有① | B.②④⑥ | C.①③④ | D.只有⑥ |
能正确表示下列化学反应的离子方程式的是
| A.金属铝溶于盐酸中:Al+2H+=Al3++H2↑ |
| B.碳酸钙溶于硝酸中:2H++CO32-=CO2↑+H2O |
| C.硫酸氢钠溶液中加入碳酸氢钠溶液:H++HCO3-=CO2↑+H2O |
| D.在澄清石灰水中通入过量的CO2:Ca2++2OH-+CO2=CaCO3↓+H2O |
已知气体的摩尔质量越小,扩散速度越快。下图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环。下列关于甲、乙的判断正确的是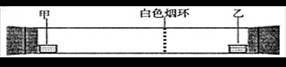
| A.甲是浓氨水,乙是浓硫酸 | B.甲是浓盐酸,乙是浓氨水 |
| C.甲是浓氨水,乙是浓硝酸 | D.甲是浓硝酸,乙是浓氨水 |