V、W、X、Y、Z是原子序数依次递减的五种常见元素。X元素是地壳中含量最多的元素,Y、Z组成的气态化合物M的水溶液呈碱性,W的单质在X2中的燃烧产物可使品红溶液褪色,V是一种历史悠久、应用广泛的金属元素。请回答:
(1)Y元素在周期表中的位置是 ;
(2)由以上五种元素两两组合所形成的常见化合物中,有一种气体物质能与水反应生成气体且反应属于氧化还原反应,请写出该反应的化学方程式 。
(3)X、Y、Z三种元素可组成一种强酸U,M在适当条件下被U吸收生成一种盐。该盐的水溶液的pH 7(填“大于”、“小于”或“等于”)。原因是(用离子方程式表示)
(4)若将V金属投入到盐酸溶液中,生成了浅绿色溶液N。N的酸性溶液与双氧水反应的离子方程式:
(5)有人设想寻求合适的催化剂和电极材料,以Y2、Z2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型原电池,放电时溶液中H+移向 (填“正”或“负”)极。
(10分)有A、B、C、D四种强电解质,它们在水中电离时可产生下列离子(每种物质只含一种阴离子且互不重复) 提示:CH3COONH4溶液为中性
| 阳离子 |
Na+、Ba2+、NH4+ |
| 阴离子 |
CH3COO-、Cl-、OH-、SO42- |
已知:①A、C溶液的pH均大于7,A、B的溶液中水的电离程度相同;
②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成刺激性气味的气体,A溶液和D溶液混合时无明显现象。
(1)A是______ ,B是_______ ,C是_______ ,D是________ 。
(2)用离子方程式表示A的水溶液显碱性的原因________________________________。
(3)25℃时,0.1mol·L-1 B溶液的pH=a,则B溶液中c(H+)-c(NH3·H2O)= _______(用含a的关系式表示)。
(4)将等体积、等物质的量浓度的B溶液和C溶液混合,反应后溶液中各种离子浓度由大到小的顺序为___________________。
用滴管将新制的饱和氯水慢慢滴入含酚酞的NaOH稀溶液中,当滴到最后一滴时红色突然褪去,试回答下列问题:
(1)实验室保存饱和氯水的方法是___________________________________________。
(2)产生上述现象的原因可能有两种(用简要文字说明)
①是由于_______________________________________________________________;
②是由于_____________________________________________________________。
简述怎样用实验证明红色褪去的原因是①或者是②:_______________________
________________________________________________________________________。
(1)将复杂硅酸盐改写成氧化物形式:KAlSi3O8:________________
(2)除杂(括号内为杂质):请把所加试剂和有关离子反应方程式填在空白处。
| 试剂 |
离子反应方程式 |
|
| ①NaHCO3溶液(Na2CO3) |
||
| ② Fe2O3(Al2O3) |
||
| ③FeCl3溶液(FeCl2) |
||
| ④CO2(HCl) |
石墨的片层结构如图所示,试回答: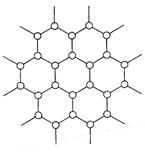
(1)平均个碳原子构成一个正六边形。
(2)石墨晶体每一层内碳原子数与碳一碳化学键之比是。
(3)ng碳原子可构成个正六边形。
金属铜的晶胞是一个“面心立方体”(注:八个顶点和六个面分别有一个金属原子)。则金属铜平均每个晶胞中有__________个金属原子组成的。已知铜的摩尔质量是64g·mol—1,金属铜的密度是8.93g·cm-3。则金属铜的晶胞体积是。计算过程为: