下列关于热化学反应的描述中正确的是( )
| A.HCl和NaOH反应的中和热ΔH=-57.3 kJ/mol,则H2SO4和Ba(OH)2反应的中和热ΔH=2×(-57.3) kJ/mol |
| B.CO(g)的燃烧热是ΔH=-283.0 kJ/mol,则2CO2(g)===2CO(g)+O2(g)反应的ΔH=+2×283.0 kJ/mol |
| C.需要加热才能发生的反应一定是吸热反应 |
| D.吸热反应中,新化学键形成吸收能量;放热反应中,新化学键形成放出能量 |
下述实验不能达到预期目的的是
| 编号 |
实验内容 |
实验目的 |
| A |
将AlCl 3溶液蒸干灼烧 |
制备Al 2O 3 |
| B |
向沸水中滴加几滴FeCl 3饱和溶液,继续加热至红褐色 |
制备Fe(OH) 3胶体 |
| C |
向某溶液中加入稀H 2SO 4,将产生的气体通入澄清石灰水 |
检验溶液中是否含有 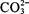 |
| D |
相同温度下,测定浓度分别为0.1 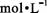 的Na 2CO 3和CH 3COONa溶液的pH 的Na 2CO 3和CH 3COONa溶液的pH |
比较  和 和 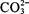 结合 结合 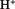 的能力强弱 的能力强弱 |
下列根据反应原理设计的应用,不正确的是
A.CO32- + H2O 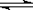 HCO3-+ OH-热的纯碱溶液清洗油污 HCO3-+ OH-热的纯碱溶液清洗油污 |
B.Al3+ + 3H2O 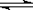 Al(OH)3 + H+明矾净水 Al(OH)3 + H+明矾净水 |
C.TiCl4+ (x+2)H2O(过量)  TiO2·x H2O↓ + 4HCl用TiCl4制备TiO2 TiO2·x H2O↓ + 4HCl用TiCl4制备TiO2 |
D.SnCl2 + H2O 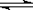 Sn(OH)Cl↓ + HCl配制氯化亚锡溶液时加入氢氧化钠 Sn(OH)Cl↓ + HCl配制氯化亚锡溶液时加入氢氧化钠 |
下列说法正确的是
①热稳定性:HF>H2O>H2S②离子半径:Na+>Mg2+>O2-
③碱性:Ca(OH)2>Mg(OH)2>NaOH
④相同物质的量浓度溶液的pH:NaOH>CH3COONa>NaCl
| A.①③ |
B.②④ |
C.①④ |
D.②③ |
Cl2是纺织工业常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”。S2O32-和Cl2反应的产物之一为SO42-。下列说法不正确的
| A.该反应中还原剂是S2O32- |
| B.H2O参与该反应,且作氧化剂 |
| C.根据该反应可判断氧化性:Cl2>SO42- |
| D.上述反应中,每生成l mol SO42-,可脱去2 mol Cl2 |
下列图像分别表示有关反应的反应过程与能量变化的关系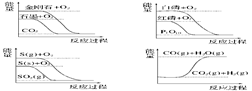
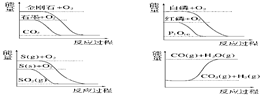
据此判断下列说法中正确的是
| A.石墨转变为金刚石是吸热反应 |
| B.白磷比红磷稳定 |
| C.S(g) ===" S(s)" ΔH > 0 |
| D.H2(g)+I2(g) ===" 2HI(g)" ΔH > 0 |