如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物。则下列说法错误的是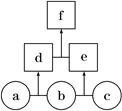
| A.常温下,单质a呈气态 | B.单质c具有强氧化性 |
| C.稳定性:d>e | D.f受热易分解为d和e |
M和N两溶液分别含有下列十二种离子中的五种和七种离子:K+、Na+、H+、NH4+、Fe3+、A13+、Cl-、OH-、NO3-、S2-、CO32-、SO42-。己知两溶液所含离子各不相同,M溶液里的阳离子只有两种,则N溶液里的阴离子应该是()
| A.OH-、CO32-、SO42- | B.S2-、Cl-、SO42- |
| C.CO32-、NO3-、S2- | D.Cl-、SO42-、NO3- |
现有一定量的铁粉和铜粉的混合物,将其平均分成四等份,分别加入同浓度不同体积的稀硝酸,充分反应后,在标准状况下生成NO的体积和剩余金属的质量如下表(假设硝酸的还原产物只有NO一种):
| 编号 |
① |
② |
③ |
④ |
| 稀硝酸体积/mL |
100 |
200 |
300 |
400 |
| 剩余金属/g |
18.0 |
9.6 |
0 |
0 |
| NO体积/mL |
2240 |
4480 |
6720 |
V |
根据上表中的数据计算分析,下列推断正确的是()
A.①中溶解了5.6 g FeB.②中溶解了9.6 g Cu
C.硝酸的浓度为4 mol/LD.④中V = 6720
下列分子结构中,原子的最外层电子能都满足8电子稳定结构的是 ( )
| A.CH4 | B.PF3 | C.SF6 | D.BeCl2 |
向硫酸铜溶液中通入足量NH3后可得到深蓝色溶液[溶质为Cu(NH3)4SO4],再向所得溶液通入SO2至溶液呈微酸性发现有白色沉淀Q生成,反应方程式为:①2Cu(NH3)4SO4+3SO2+4H2O=2NH4CuSO3↓+3(NH4)2SO4。再将Q与足量的10mol/L硫酸混合微热,则会发生如下反应:②2NH4CuSO3+2H2SO4=Cu+(NH4)2SO4+2SO2+CuSO4+2H2O。下面有关分析中正确的是()
A.①是非氧化还原 反应,而②是氧化还原反应 反应,而②是氧化还原反应 |
| B.上述反应中SO2的作用只相当于催化剂 |
| C.反应②中CuSO4是氧化产物 |
| D.反应①中SO2发生还原反应 |
已知在pH为4~5的环境中,Cu2+、Fe2+几乎不水解,而Fe3+几乎完全水解。工业上制CuCl2是将浓盐酸用蒸气加热到80℃左右,再慢慢加入粗氧化铜(含少量杂质FeO),充分搅拌使之溶解。欲除去溶液中的杂质离子,下述方法中可行的是()
| A.加入纯Cu将Fe2+还原为Fe |
| B.向溶液中通入H2S使Fe2+沉淀 |
| C.向溶液中通入Cl2,再通入NH3,调节pH值为4~5 |
| D.向溶液中通入Cl2,再加入纯净的CuO粉末调节pH值为4~5 |