如图,图1为甲烷和O2构成的燃料电池,图2为电解MgCl2溶液装置。用该装置进行实验,反应开始后,观察到x电极附近出现白色沉淀。下列说法正确的是 ( ) 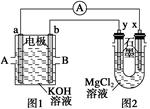
| A.A处通入的气体为O2,B处通入的气体为CH4 |
| B.电池内部K+向b极移动,OH-向a极移动 |
| C.图1装置中发生的总反应为:CH4+2O2===CO2+2H2O |
| D.图1、图2中电解质溶液的pH均增大 |
下列说法正确的是
| A.纤维素和淀粉遇碘水均显蓝色 |
| B.蛋白质、乙酸和葡萄糖均属电解质 |
| C.乙酸乙酯和食用植物油均可水解生成乙醇 |
| D.红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物结构的分析 |
亚氨基羟(Li2NH)是一种储氢容量器,安全性好的固体储氢材料,其储氢原理可表示为
Li2NH+H2=LiNH2+LiH。
下列有关说法正确的是
| A.Li2NH中N的化合价是-1 | B.该反应中H2既是氧化剂又是还原剂 |
| C.Li+和H+的离子半径相等 | D.此法储氢和钢瓶储氢的原理相同 |
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是
| A.含有碳碳双键、羟基、羰基、羧基 |
| B.含有苯环、羟基、醛基、羧基 |
| C.含有羟基、羰基、羧基、酯基 |
| D.含有碳碳双键、苯环、酯基、羰基 |
下列各组有机物只用一种试剂无法鉴别的是
| A.乙醇、甲苯、硝基苯 | B.苯、苯酚、己烯 | C.苯、甲苯、环己烷 | D.甲酸、乙醛、乙酸 |
下列各化合物的命名中正确的是