已知X、Y元素同周期,且电负性X>Y,下列说法错误的是 ( )
| A.X与Y形成化合物时,X显负价,Y显正价 |
| B.第一电离能可能Y小于X |
| C.最高价含氧酸的酸性:X对应酸的酸性弱于Y对应酸的酸性 |
| D.气态氢化物的稳定性:HmY小于HmX |
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解质溶液在电解质溶液在电解质储罐和电池间不断循环.下列说法不正确的是
| A.阳离子交换膜可阻止Br2与Zn直接发生反应 |
| B.放电时正极的电极反应式为Br2+2e-=2Br- |
| C.充电时电极b连接电源的正极 |
| D.放电时左侧电解质储罐中的离子总浓度增大 |
氰(CN)2,硫氰(SCN)2等称为拟卤素,与卤素单质性质相似,它们的阴离子与也卤素阴离子性质相似,阴离子的还原性顺序为: Cl-<Br-<CN-<SCN-<I-,又知,拟卤素形成的无氧酸和含氧酸一般为弱酸,下列反应中,不合理的是
A.4HCN(浓)+MnO2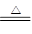 Mn(CN)2+(CN)2↑+2H2O Mn(CN)2+(CN)2↑+2H2O |
| B.(CN)2+H2O=2H++CN-+CNO- |
| C.(CN)2+2OH-=CN-+CNO-+H2O |
| D.(CN)2+2SCN-=2CN-+(SCN)2 |
已知NH4CuSO3与足量的5 mol•L-1硫酸溶液混合微热,产生下列现象::①有红色金属生成②产生刺激性气味的气体 ③溶液呈现蓝色.据此判断下列说法正确的是
| A.反应中硫酸作氧化剂 |
| B.NH4CuSO3中硫元素被氧化 |
| C.刺激性气味的气体是氨气 |
| D.1mol NH4CuSO3完全反应转移0.5mol电子 |
已知:NH3·H2O(aq)与H2SO4(aq)反应生成1mol正盐的△H=-24.2kJ•mol-1,强酸、强碱稀溶液反应的中和热为△H=-57.3kJ•mol-1,则NH3·H2O在水溶液中电离的△H等于
| A.-69.4 kJ/mol | B.-45.2kJ/mol | C.+69.4 kJ/mol | D.+45.2 kJ/mol |
化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是
A.根据图①可判断可逆反应A2(g)+3B2(g) 2AB3(g)的△H>0 2AB3(g)的△H>0 |
B.图②表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强大 3C(g)+D(s)的影响,乙的压强大 |
| C.图③表示在含等物质的量NaOH、Na2CO3的混合溶液中逐滴加入0.1mol/L盐酸至过量时,产生气体的物质的量与消耗盐酸的体积关系 |
| D.图④表示Cl2通入H2S溶液中pH变化 |