向等质量的两份锌粉a和b中,分别加入过量的稀H2SO4,同时a中加入少量CuSO4溶液,图中产生氢气的体积(V)与时间(t)的关系基本正确的是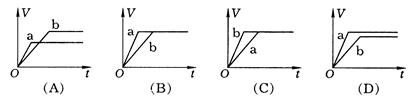
下列关于蛋白质在人体中的新陈代谢的认识不正确的是
| A.蛋白质溶液里加(NH4)2SO4溶液可提纯蛋白质 |
| B.在豆浆中加入少量石膏能使豆浆凝结为豆腐 |
| C.温度越高,酶对某些化学反应的催化效率越高 |
| D.鉴别某纺织物成分是蚕丝还是人造丝,可采用灼烧闻气味的方法 |
近期在西非国家爆发的埃博拉疫情呈加速蔓延之势,已知该病毒对化学药品敏感,乙醇、高锰酸钾溶液、次氯酸钠溶液、双氧水等消毒剂可以完全灭活病毒感染性。下列有关说法正确的是
| A.乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的 |
| B.高锰酸钾溶液和双氧水的消毒原理相同 |
| C.双氧水具有较强的腐蚀性,不能用于皮肤的消毒 |
| D.在次氯酸钠溶液中通入少量二氧化硫可得到亚硫酸钠和次氯酸 |
重金属盐能使人体中毒,这是由于它使人体内的蛋白质
| A.发生了水解作用 | B.发生了盐析作用 |
| C.发生了变性作用 | D.发生了分解作用 |
下列有关肥皂的叙述中错误的是
| A.肥皂与纯碱的去污原理相同 |
| B.肥皂可以加速油污在水中的分散 |
| C.肥皂是油脂在碱性条件下水解生成的 |
| D.肥皂主要成分的分子中含有亲油基团和亲水基团 |
将硬脂酸甘油酯与NaOH溶液共热后进行皂化反应后,能把硬脂酸钠和甘油从混合物中 分离出来的操作为
①盐析,②过滤,③蒸馏,④分液,⑤结晶
| A.①②③ | B.①③④⑤ | C.②③④ | D.①②④⑤ |