豆类作物中含有的天然蛋白质在酶的作用下,水解生成A、B两种有机物。其中A的化学式为C4H7O4N,B的化学式为C6H14O2N2;已知A、B的分子结构中均不含甲基,且链端都有官能团。
(1)A的结构简式为:_______________________________________________________;
B的结构简式为:_________________________________________________________。
(2)题中酶的作用是_______________________________________________________;
影响其作用的主要因素有_________________________________________________。
(共12分)原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)Z原子的核外电子排布为 ;
(2)化合物甲由元素X与Y组成,1mol甲含18mol电子,请写出甲的电子式:;
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,其离子方程式为。
(4)已知离子化合物乙由X、Y、Z、W四种元素组成,乙既能与盐酸反应,又能与氯水反应,1mol 乙能与过量NaOH浓溶液反应,最多可生成22.4L气体(标准状况)。写出加热条件下乙与过量NaOH溶液反应的离子方程式。
(5)用亚硝酸氧化化合物甲,可生成氮的另一种氢化物,该氢化物的相对分子质量为43,其中氮原子的质量分数为97.7%,该氢化物的分子式为。该氢化物受撞击时完全分解为氮气和氢气,则2.15g该氢化物受撞击后产生的气体在标况下的体积为L。
( 8分)原子序数小于36的X、Y、Z、W四种元素,其中X形成的阳离子就是一个质子,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29。
回答下列问题:
(1)Y2X2分子中Y原子轨道的杂化类型为,
1mol Y2X2含有σ键的数目为。
(2)化合物ZX3的沸点比化合物YX4的高,其主要原因是。
(3)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是。
原子结构与元素周期表存在着内在联系。根据已学原子结构及晶体知识,请回答下列问题:
(1)具有(n-1)d10ns2电子构型的元素位于周期表中族。
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为:。
(3)写出铝元素原子的核外电子排布式。
(4)写出3p轨道上有2个未成对电子的元素的符号:。
(1)写出表示含有8个质子、10个中子的原子的化学符号。
(2)元素周期表中,所含元素超过18种的周期是。
(3)葡萄糖的结构简式是
下列A~H 八种物质存在如下图所示的转化关系(反应条件、部分产物未标出)。已知A是正盐,B能使品红溶液褪色,G是红棕色气体。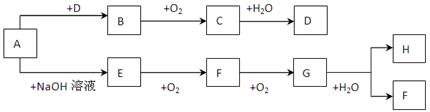
试回答下列问题:
(1)写出下列各物质的化学式 A
(2)按要求写出下列反应的有关方程式
E→F反应的化学方程式;
G→H反应的离子方程式。
(3)写出H的浓溶液与木炭反应的化学方程式。
(4)检验D中阴离子的方法是