以2—氯丙烷为主要原料制1,2—丙二醇CH3CH(OH)CH2OH时,经过的反应为( )
| A.加成—消去—取代 | B.消去—加成—取代 |
| C.取代—消去—加成 | D.取代—加成—消去 |
苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+,现榨的苹果汁在空气中会由淡绿色变为黄色(Fe3+)。若榨汁时加入维生素C,可有效防止这种现象发生,这说明维生素C具有
| A.氧化性 | B.还原性 | C.碱性 | D.酸性 |
常温下,下列各组离子在指定溶液中能大量共存的是
| A. |
 的溶液中: 的溶液中:
 、 、
 、 、
 、 、

|
| B. |
由水电离的
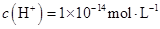 的溶液中: 的溶液中:
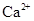 、 、
 、 、
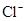 、 、

|
| C. |
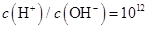 的溶液中: 的溶液中:
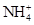 、 、
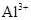 、 、
 、 、
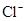
|
| D. |
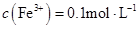 的溶液中: 的溶液中:
 、 、
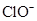 、 、
 、 、

|
常温下,在盛有溴水的三支试管中分别加入三种无色的液态有机物,振荡后静置,出现如下图所示现象,则加入的三种有机物可能正确的一组是
| A.①是溴乙烷,②是环己烷,③是酒精 |
| B.①是甘油,②是溴苯,③是汽油 |
| C.①是苯,②是CCl4,③是酒精 |
| D.①是甲苯,②是乙酸,③是苯酚 |
2011年6月4日晚上22时55分左右,杭州市辖区建德境内杭新景高速公路发生苯酚槽罐车泄漏事故,导致部分苯酚泄漏并造成污染。对泄漏的苯酚,你认为下列措施中哪个方法最佳:
| A.用水冲洗掉 | B.用稀盐酸洗掉 | C.用酒精冲洗掉 | D.用石灰中和 |
除去括号内杂质所用试剂和方法,正确的是
A.乙醇(乙酸) 溶液分液 溶液分液 |
B.乙烯(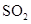 ) ) 溶液洗气 溶液洗气 |
| C.乙烷(乙烯) H2(催化剂)催化加氢 |
D.乙醇(水) 蒸馏 蒸馏 |