短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y、Z原子序数之和是W的2倍,X、Z在周期表中的相对位置如图所示,X的最低负价绝对值与其原子最外层电子数相等。下列说法不正确的是
| A.原子半径:Y>Z>W | B.一定条件下,Y可置换出X |
| C.气态氢化物稳定性:Z>W | D.熔点YW2>XW4 |
原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,X、Z的最外层电子数之和与Y、W的最外层电子数之和相等。甲的化学式为YX3,是一种刺激性气味的气体,乙是由X、Y、Z组成的盐。下列说法正确的是
| A.由X、Y、Z组成盐的水溶液呈酸性,则溶液中该盐阳离子浓度小于酸根离子浓度 |
| B.YX3的水溶液呈弱碱性,能使湿润的蓝色石蕊试纸变红 |
| C.原子半径:Z<Y<W,而简单离子半径:W<Y<Z |
| D.W的氯化物熔点低,易升华,但水溶液能导电,由此推断它属于弱电解质 |
设NA为阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,2.24LCl2溶于水,转移的电子数目为0.1NA |
| B.常温下,10 L pH=12的Na2CO3溶液中含有的OH-离子数为0.1NA |
| C.标准状况下,22.4 LNO2和NO的混合气体中所含的氮原子总数为2NA |
| D.将含有1molFeCl3的浓溶液完全水解可得到Fe(OH)3胶粒的数目为 NA |
常温下,向l00mL 0.01 mol•L-1盐酸中逐滴加入0.02 mol•L-1 MOH溶液,如下图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是()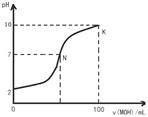
| A.MOH是弱碱 |
| B.N点c(Cl-) = c(M+) |
C.随着MOH溶液的滴加,比值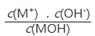 不变 不变 |
| D.K点对应的溶液c(MOH)+c(OH-)-c(H+) = 0.005 mol•L-1 |
甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用。某型甲醇燃料电池的总反应式2CH4O + 3O2 = 2CO2↑+ 4H2O,下图是该燃料电池的示意图。下列说法错误的是()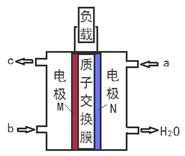
| A.燃料电池将化学能转化为电能 |
| B.a是甲醇、b是氧气 |
| C.质子从M电极区穿过交换膜移向N电极区 |
| D.负极反应:CH4O - 6e- + H2O = CO2↑+ 6H+ |
在密闭容器中进行反应:X(g)+3Y(g)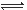 2Z(g),下列说法正确的是 ( )
2Z(g),下列说法正确的是 ( )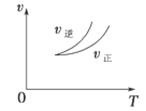

| A.左上图说明正反应为吸热反应 |
| B.反应达平衡后,增大压强气体密度将减小 |
| C.右上图可表示升高温度使平衡向逆反应方向移动 |
| D.右上图虚线可表示使用催化剂后引发的反应速率变化 |