(15分)碱式碳酸铜的成分有多种,其化学式一般可表示为xCu(OH)2·yCuCO3。
(1)孔雀石呈绿色,是一种名贵的宝石,其主要成分是Cu(OH)2·CuCO3。某兴趣小组为探究制取孔雀石的最佳反应条件,设计了如下实验:
实验1:将2.0mL 0.50 mol·L—1的Cu(NO3)2溶液、2.0mL 0.50 mol·L—1的NaOH溶液和0.25 mol·L—1的Na2CO3溶液按表Ⅰ所示体积混合。
实验2:将合适比例的混合物在表Ⅱ所示温度下反应。
实验记录如下:
| 编号 |
V (Na2CO3)/ mL |
沉淀情况 |
|
编号 |
反应温度/℃ |
沉淀情况 |
| 1 |
2.8 |
多、蓝色 |
|
1 |
40 |
多、蓝色 |
| 2 |
2.4 |
多、蓝色 |
|
2 |
60 |
少、浅绿色 |
| 3 |
2.0 |
较多、绿色 |
|
3 |
75 |
较多、绿色 |
| 4 |
1.6 |
较少、绿色 |
|
4 |
80 |
较多、绿色(少量褐色) |
表Ⅰ 表Ⅱ
①实验室制取少许孔雀石,应该采用的条件是 。
②80℃时,所制得的孔雀石有少量褐色物质的原因是 。
(2)实验小组为测定上述某条件下所制得的碱式碳酸铜样品组成,利用下图所示的装置(夹持仪器省略)进行实验:
步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中。
步骤2:打开活塞K,鼓入空气,一段时间后关闭,称量相关装置的质量。
步骤3:加热装置B直至装置C中无气泡产生。
步骤4: 。
步骤5:称量相关装置的质量。
①装置A的作用是 ;若无装置E,则实验测定的x/y的值将 (选填“偏大”、“偏小”或“无影响”)。
②某同学在实验过程中采集了如下数据:
A.反应前玻璃管与样品的质量163.8g
B.反应后玻璃管中残留固体质量56.0g
C.装置C实验后增重9.0g
D.装置D实验后增重8.8g
为测定x/y的值,你认为可以选用上述所采集数据中的 (写出所有组合的字母代号)一组即可进行计算,并根据你的计算结果,写出该样品组成的化学式 。
某学生用0.200 0 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线以下某一刻度,并记下读数
④移取20.00 mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数
请回答:
(1)以上步骤有错误的是(填编号),该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”)。
(2)判断滴定终点的现象是:锥形瓶中溶液从色变为色,且半分钟内不变色。
(3)如图是某次滴定时的滴定管中的液面,其读数为mL。
(4)根据下列数据:请计算待测盐酸溶液的浓度为mol/L
| 滴定次数 |
待测液体积(mL) |
标准NaOH溶液读数记录(mL) |
|
| 滴定前读数 |
滴定后读数 |
||
| 第一次 |
20.00 |
0.40 |
20.40 |
| 第二次 |
20.00 |
4.00 |
24.00 |
| 第三次 |
20.00 |
2.00 |
24.10 |
某化学课外活动小组在实验室设计了如图所示的实验装置,进行“氨的催化氧化”实验。
(1)A处是气体发生装置,A中所用的试剂只能从下列物质中选取:
①硝酸铵;②碳酸铵;③碳酸氢铵;④氯化铵;⑤熟石灰;⑥氢氧化钠。
若A中制取气体时只用了一种药品,则该药品可以是(填选项编号),在只用一种药品制取氨气时,图中空白处所需仪器应为(选填下列仪器编号,固定装置省略)。
(2)该装置补充完整后,仍然存在一定的缺陷,试从安全与环保的角度来考虑,对该装置进行改进:
①;
②。
(3)按照改进后的装置进行实验,请完成以下问题:
①装置B的作用是;
②写出C中发生反应的化学方程式:;
③若A、B处试剂足量,则装置D中可以观察到的实验现象有。
实验室里常见到如图所示仪器,该仪器为两头密封的玻璃管,中间带有一根玻璃短柄。该仪器可进行多项实验,当玻璃管内装有碘晶体时,用此仪器可进行碘升华实验,具有装置简单,操作方便,现象明显,没有污染,可反复使用等优点。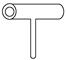
(1)用此仪器不能反复进行的实验是。
A.NH4Cl固体受热分解
B.KMnO4晶体受热分解
C.白磷和红磷在一定温度下互相转变
(2)如果玻璃管内装有某种红色溶液,加热时溶液颜色变浅,冷却时恢复红色,该溶液可能是;如果玻璃管内封有无色溶液,加热溶液时,溶液变红,冷却后恢复原颜色,此溶液可能是。
一定量的浓硫酸与足量Zn充分反应时,有SO2和H2生成。某校化学研究性学习小组分别从定性和定量两方面对此作了研究。
定性实验:按图组装好实验装置,微热试管A,观察实验现象。反应开始后,观察到A试管中Zn与浓硫酸反应,C、D、E中有气泡产生,随后气泡量减少,品红溶液褪色,D中先出现浑浊后浑浊消失。反应较长时间后,C、D、E中的气泡量又会明显增加。试回答下列问题: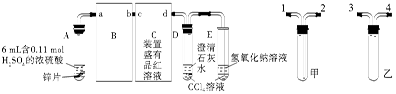
(1)从甲、乙装置选择合适的填入B、C中,并进行正确连接,a接、接b,c接、接d;D、E两支试管中CCl4的作用是。
(2)能证明浓硫酸具有强氧化性的实验现象为;反应较长时间后气泡量又会明显增加的原因是。
(3)一定量的浓硫酸与足量Zn充分反应时,有H2生成的理由是;实验过程中,浓硫酸表现强氧化性的反应方程式是。D中浑浊消失的离子反应方程式是。
定量实验:某化学实验研究性学习小组设计了以下实验,以定量测定反应中生成的SO2和H2的体积之比。
取A试管中充分反应后的溶液2 mL(假设反应前后溶液的体积不变),配制成100 mL溶液。然后取稀释液20.00 mL滴加BaCl2溶液使沉淀完全,过滤、洗涤、干燥沉淀,称量所得沉淀为1.4 g。
(4)完成定量实验部分所需的玻璃仪器有:滴管、玻璃棒、烧杯、量筒、干燥器、、、、、等(可填满,也可以空缺)。
(5)计算反应中生成的SO2和H2的体积之比:。
二氧化锰与浓盐酸混合加热得到氯气,如图是制取并探究Cl2化学性质的装置图。
(1)圆底烧瓶中发生反应的化学方程式为。
(2)若要得到干燥纯净的气体,B、C中应分别盛放的试剂为、。
(3)E中若装有FeCl2溶液,反应的离子方程式为,E中若装有淀粉碘化钾溶液,能观察到的实验现象是。
(4)实验中发现:浓盐酸与MnO2混合加热生成氯气,稀盐酸与MnO2混合加热不生成氯气。针对上述现象某化学兴趣小组对“影响氯气生成的原因”进行了讨论,并设计了以下实验方案:
a.稀盐酸滴入MnO2中,然后通入HCl气体加热
b.稀盐酸滴入MnO2中,然后加入NaCl固体加热
c.稀盐酸滴入MnO2中,然后加入浓硫酸加热
d.MnO2与NaCl的浓溶液混合加热
e.浓硫酸与NaCl固体、MnO2固体共热
①实验b的目的是,实验c的目的是。
②实验现象:a、c、e有黄绿色气体生成,b、d没有黄绿色气体生成。由此得出影响氯气生成的原因是 。