Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法错误的是( )
| A.Mg 电极是该电池的负极 |
| B.溶液中Cl-向石墨电极移动 |
| C.该装置中电子从Mg电极流向石墨电极 |
| D.H2O2在石墨电极上发生还原反应 |
将质量分数为0.052 (5.2%)的NaOH溶液1L(密度为1.06 g/cm3),用Pt电极进行电解,当溶液中NaOH的质量分数改变了0.010(1.0 %)时,停止电解,则此时溶液中应符合的关系是()
| NaOH的质量分数 |
阳极析出物质的质量/g |
阴极析出物质的质量/g |
|
| A |
0.062(6.2%) |
19 |
152 |
| B |
0.062(6.2%) |
152 |
19 |
| C |
0.042(4.2%) |
1.2 |
9.4 |
| D |
0.042(4.2%) |
9.4 |
1.2 |
将右图所示实验装置的 K 闭合,下列判断正确的是()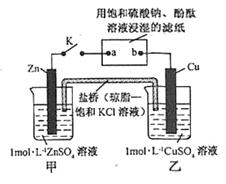
| A.Cu 电极上发生还原反应 |
| B.电子沿 Zn→a→b→Cu 路径流动 |
| C.片刻后甲池中c(SO42-)增大 |
| D.片刻后可观察到滤纸b点变红色 |
纽扣电池的两极材料分别为锌和氧化银,电解质溶液为KOH溶液。放电时两个电极反应分别为: Z n +2OH--2e-= Zn(OH)2,Ag2O+ H2O+ 2e-= 2Ag +2OH-
下列说法正确的是:()
| A.溶液中OH-向正极移动,K+、H+向负极移动 |
| B.锌发生还原反应,氧化银发生氧化反应 |
| C.锌是负极,氧化银是正极 |
| D.在电池放电过程中,负极区溶液碱性增强 |
下图所示装置中观察到电流计指针偏转,M棒变粗,N棒变细,指针指向M,由此判断下表中所列M、N、P物质,其中可以成立的组合是()
关于下列装置说法正确的是()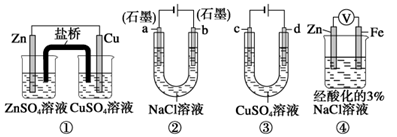
| A.装置①中,盐桥中的K+移向ZnSO4溶液 |
| B.装置②工作一段时间后,a极附近溶液的pH增大 |
| C.用装置③精炼铜时,c极为粗铜 |
| D.装置④中电子由Zn流向Fe,装置中有Fe2+生成 |