在2009年10月1日,新的饮用矿泉水强制性国家标准《饮用天然矿泉水》正式实施,其中“溴酸盐(BrO3-)”这一潜在致癌物质被做了严格限制。有关专家解释,矿泉水在开采过程中会含有少量溴化物(Br-),在后续的生产过程中经臭氧(O3)处理逐渐转化成溴酸盐。下列有关该转化过程的认识正确的是( )
| A.该过程中溴化物(Br-)得到电子 |
| B.该过程中臭氧(O3)是氧化剂,溴酸盐(BrO3-)是还原剂 |
| C.该过程中溴元素被还原,氧元素被氧化 |
| D.该过程中溴元素发生氧化反应,氧元素发生还原反应 |
按下图装置,持续通入X气体,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体是
| A.H2 | B.CO和H2 | C.NH3 | D.CH3CH2OH(气) |
将甲苯与液溴混合加入铁粉,其反应产物可能为
①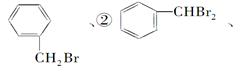

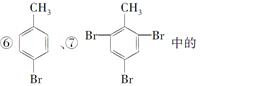
| A.①②③ | B.⑦ | C.全部都有 | D.④⑤⑥⑦ |
有机物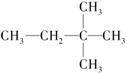 与氯气发生取代反应,生成的一氯代物有
与氯气发生取代反应,生成的一氯代物有
| A.1种 | B.2种 | C.3种 | D.4种 |
下列说法正确的是
| A.相对分子质量相同的物质是同种物质 |
| B.分子式相同的不同有机物一定是同分异构体 |
| C.具有同一通式的物质属于同系物 |
| D.同分异构现象只存在于有机物中 |
2SO2(g)+O2(g) 2SO3(g)的反应中,经过一段时间后,SO3的浓度增加了0.9mol/L,此时间内用O2表示的平均速率为0.45mol/(L·s),则这段时间是
2SO3(g)的反应中,经过一段时间后,SO3的浓度增加了0.9mol/L,此时间内用O2表示的平均速率为0.45mol/(L·s),则这段时间是
| A.1 s | B.0.44 s | C.2 s | D.1.33 s |