下列事实能说明NH3·H2O一定是弱电解质的是
①常温下,NH3·H2O溶液能使酚酞变红; ②用NH3·H2O溶液做导电性实验,灯泡很暗;
③常温下,0.1mol / L氯化铵溶液的pH约为5
④常温下,体积相同且pH相同的NH3·H2O溶液和NaOH溶液,与相同浓度的HCl溶液中和时,消耗HCl溶液的体积:前者>后者
| A.①②③④ | B.②③④ | C.③④ | D.②④ |
下列物质中,既含有离子键,又含有共价键的是()
| A.MgCl2 | B.NH4Cl | C.Na2O | D.H2O2 |
已知气体的摩尔质量越小,扩散速度越快。下图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环。下列关于物质甲、乙的判断正确的是()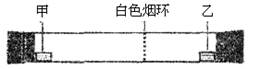
| A.甲是浓氨水,乙是浓硫酸 | B.甲是浓盐酸,乙是浓氨水 |
| C.甲是浓氨水,乙是浓盐酸 | D.甲是浓硝酸,乙是浓氨水 |
某元素原子L层电子数比K层电子数多5个,该元素的最高正价为()
| A.+7 | B.+5 | C.+3 | D.无最高正价 |
下列过程中,涉及化学变化的是()
| A.氯气通入水中制氯水 | B.蒸馏法将海水淡化为饮用水 |
| C.活性炭使红墨水褪色 | D.四氯化碳萃取碘水中的碘 |
下列气体中,与酸雨密切相关的是()
①NO2②CO2③SO2④CO
| A.③ | B.①③ | C.①② | D.③④ |