橙花醇具有玫瑰及苹果香气,可作为香料,其结构简式如下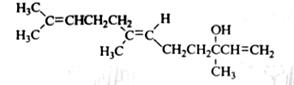
下列关于橙花醇的叙述,错误的是( )
| A.既能发生取代反应,也能发生加成反应 |
| B.在浓硫酸催化下加热脱水,可生成不止一种四烯烃(分子中含有四个碳碳双键的烯烃) |
| C.1mo1橙花醇在氧气中充分燃烧,需消耗470.4L氧气(标准状况) |
| D.1mo1橙花醇在室温下与溴的四氯化碳溶液反应,最多消耗240g溴 |
白磷与氧可发生如下反应:P4+5O2="==" P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P:a kJ·mol-1、P-O:b kJ·mol-1、P=O:c kJ·mol-1、O=O:d kJ·mol-1,根据
 图示的分子结构和有关数据估算该反应的
图示的分子结构和有关数据估算该反应的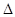 H,其中正确的是
H,其中正确的是
| A.(6a+5d-4c-12b) kJ·mol-1 | B.(4c+12b-6a-5d) kJ·mol-1 |
| C.(4c+12b-4a-5d) kJ·mol-1 | D.(4a+5  d-4c-12b) d-4c-12b)  kJ·mol-1 kJ·mol-1 |
已知在298K时下述反应的有关数据:C(s)+ O2(g)===CO(g)△H1 = -110.5 kJ• mol-1 C(s)+O2(g) ===CO2(g)△H2= -393.5 kJ• mol-1则C(s)+CO2(g)===2CO(g) 的△H 为
O2(g)===CO(g)△H1 = -110.5 kJ• mol-1 C(s)+O2(g) ===CO2(g)△H2= -393.5 kJ• mol-1则C(s)+CO2(g)===2CO(g) 的△H 为
| A.+283.5 kJ• mol-1 | B.+172.5 kJ• mol-1 | C.-172.5 kJ• mol-1 | D.-504 kJ• mol-1 |
在恒温恒容的密闭容器中,对于可逆反应A(g)+B(g)  2C(g),可以判断达到化学平衡状态的是
2C(g),可以判断达到化学平衡状态的是
A.体系压强不变  |
B.单位时间消耗n molA,同时生成2nmolC |
| C.A的转化率不变 | D.容器内气体密度不变 |
在10℃时某化学反应速率为0.1mol/ (L·s),若温度每升高10℃反应速率增加到原来的2倍。为了把该反应速率提高到1.6 mol/(L·s),则该反应需在什么温度下进行
(L·s),若温度每升高10℃反应速率增加到原来的2倍。为了把该反应速率提高到1.6 mol/(L·s),则该反应需在什么温度下进行
| A.30℃ | B.40℃ | C.50℃ | D.60℃ |
如图所示,△H1=-393.5 kJ•mol-1,△H2=-395.4 kJ•mol-1,下列说法或表示式正确的是
| A.C(s、石墨)==C(s、金刚石)△H=" +1.9" kJ•mol-1 |
| B.石墨和金刚石的转化是物理变化 |
| C.金刚石的稳定性强于石墨 |
D.1 mol石墨的总键能比1 mol金刚石 的总键能小1.9 kJ 的总键能小1.9 kJ |