下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
| |
|
|
|||||
| |
|
|
a |
|
|
|
|
| |
b |
|
c |
|
|
d |
|

(1)元素b的基态原子电子排布式为 。
(2)第三周期8种元素按单质熔点高低的排列顺序如右图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填右图中的序号)。
(3)元素a、c分别与元素d形成的化合物中,熔点较高的是(填化学式)。
香草醛结构简式为: ,请按要求完成下列问题:
,请按要求完成下列问题:
(1)香草醛有多种同分异构体,其中苯环上的一溴代物只有两种且属于芳香酸的结构简式___________;
(2)香草醛的同分异构体中属于芳香酯有种。其中某些酯与NaOH作用只能消耗等物质的量的NaOH,写出符合该条件的一种酯在NaOH溶液中水解的化学方程式:。
(3)写出香草醛发生银镜反应的化学方程式:______________________________。
(3分)肉桂醛的结构为: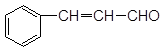
①把足量肉桂醛加入到溴水中,溴水褪色了,这____________(填“能”或“不能”)说明肉桂醛中存在碳碳双键。
②检验分子中碳碳双键的方法是_______________。
(3分)在硫酸铜溶液中加入过量的氢氧化钠溶液后,再滴入足量乙醛溶液,加热。实验过程中发生的反应的化学方程式为。
(l)常温下,如果取0.1mol•L﹣1HA溶液与0.1mol•L﹣1NaOH溶液等体积混合,测得混合液的pH=8.混合液中由水电离出的OH﹣浓度与0.1mol•L﹣1NaOH溶液中由水电离出的OH﹣浓度之比为_________ .
(2)相同温度下,将足量硫酸钡固体分别放入相同体积的①0.1mol•L﹣1硫酸铝溶液 ②0.1mol•L﹣1氯化钡溶液 ③蒸馏水 ④0.1mol•L﹣1硫酸溶液中,Ba2+浓度由大到小的顺序是_________ .(用序号填写)
(3)常温下,将a mol•L﹣1的氨水与0.1mol•L﹣1的盐酸等体积混合,当溶液中c(NH4+)=c(Cl﹣)时,用含a的代数式表示NH3•H2O的电离常数Kb= _________ mol•L﹣1.
在标准状况下,取甲、乙、丙各30.0mL 相同浓度的盐酸,然后分别慢慢加入组成相同的镁铝合金粉末,得下表中有关数据(假设反应前后溶液体积不发生变化):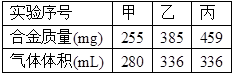
请回答:
(1)甲组实验中,盐酸(选填“过量”、“适量”或“不足量”,下同)__________________;乙组实验中盐酸______________。
(2)盐酸的物质的量浓度为_____________。
(3)合金中Mg. Al 的物质的量之比为_______________。