下列事实一定能证明HNO2是弱电解质的是( )
①常温下NaNO2溶液的pH大于7 ②用HNO2溶液做导电实验,灯泡很暗
③HNO2和NaCl不能发生反应 ④常温下0.1 mol·L-1 HNO2溶液的pH=2.1
⑤常温下pH=3的 HNO2溶液和pH=11的NaOH溶液等体积混合,pH小于7
⑥常温下pH=2的 HNO2溶液稀释至100倍,pH约为3.1
| A.①④⑥ | B.①②④⑤⑥ | C.①④⑤⑥ | D.全部 |
已知R2+离子核外有a个电子,b个中子。表示R原子符号正确的是( )
A. |
B. |
C. |
D. |
下列说法正确的是()
| A.NaCl固体中含有共价键 |
| B.CO2分子中含有离子键 |
C. 、 、 、 、 是碳的三种核素 是碳的三种核素 |
D.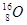 、 、 、 、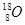 含有相同的中子数 含有相同的中子数 |
含硒(Se)的保健品已开始进入市场。已知硒与氧、硫同主族,与溴同周期,则下列关于硒的叙述中,正确的是(
| A.非金属性比硫强 | B.氢化物比HBr稳定 |
| C.原子序数为34 | D.最高价氧化物的水化物显碱性 |
下列各组元素性质递变情况错误的是
| A.Li、Be、B原子最外层电子数逐渐增多 |
| B.N、O、F原子半径依次增大 |
| C.P、S、Cl最高正价依次升高 |
| D.Li、Na、K、Rb的金属性依次增强 |
元素性质呈周期性变化的决定因素是
| A.元素原子半径大小呈周期性变化 | B.元素相对原子质量依次递增 |
| C.元素原子最外层电子排布呈周期性变化 | D.元素的最高正化合价呈周期性变化 |