(1)常温下,有0.1mol/L的盐酸和0.1mol/L的醋酸溶液,回答下列问题:
①比较两溶液的pH,盐酸 (填“<”、“=”或“>”)醋酸,写出醋酸电离的方程式 。
②两种酸均能与氢氧化钠反应生成盐,其中醋酸与氢氧化钠反应能生成醋酸钠,实验室现有部分醋酸钠固体,取少量溶于水,溶液呈 性(填“酸” 、“中” 或 “碱”),其原因是(用离子方程式表示) 。
(2)向盛有1 mL 0.1 mol/L MgCl2溶液的试管中滴加2滴2mol/L NaOH溶液,有白色沉淀生成,再滴加2滴0.1mol/LFeCl3溶液,静置。可以观察到的现象是 ,产生该现象的原因是(用离子方程式表示) 。
下图为将Zn投入一定浓度体积的H2SO4中,解释图像的成因(纵坐标为H2的生成速率)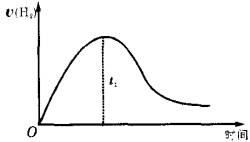
试将外界条件对化学反应速率的影响结果填入下表中。
KClO3与NaHSO3间的氧化还原反应生成Cl-和 的速率与时间关系如下图,已知反应速率随c(H+)的增加而加快,试说明
的速率与时间关系如下图,已知反应速率随c(H+)的增加而加快,试说明
(1)为什么反应开始时,反应速率增大?
(2)反应后期,反应速率逐渐降低的主要原因是___________。
合成氨反应,在其他条件不变,增大体系压强10倍,化学反应速率可增大___________倍。
在2L密闭容器中发生下列反应:

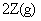 ,若最初加入的X、Y、Z都是2mol,反应中X的平均反应速率为0.12 mol/L·s,若要产物Z为2.6mol,反应需要的时间为___________。
,若最初加入的X、Y、Z都是2mol,反应中X的平均反应速率为0.12 mol/L·s,若要产物Z为2.6mol,反应需要的时间为___________。