在恒温恒容容器中进行反应A(g) 2B(g)+C(g),若A的浓度由0.1 mol·L
2B(g)+C(g),若A的浓度由0.1 mol·L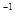 降到0.06 mol·L
降到0.06 mol·L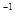 需20 s,那么由0.06 mol·L
需20 s,那么由0.06 mol·L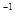 降到0.024 mol·L
降到0.024 mol·L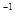 需要的时间
需要的时间
A.等于18s B,等于12s C,小于18s D.大于18s
放射性同位素钬 的原子核内的中子数与核外电子数之差是
的原子核内的中子数与核外电子数之差是
| A.32 | B.67 | C.99 | D.166 |
下列分子或离子的空间构型为平面三角形的是( )
| A.NO | B.NH3 | C.H3O+ | D.CO2 |
氨气分子空间构型是三角锥形,而甲烷是正四面体形,这是因为 ()
| A.两种分子的中心原子的杂化轨道类型不同,NH3为sp2型杂化,而CH4是sp3型杂化。 |
| B.NH3分子中N原子形成三个杂化轨道,CH4分子中C原子形成4个杂化轨道。 |
| C.NH3分子中有一对未成键的孤对电子,它对成键电子的排斥作用较强。 |
| D.氨气分子是极性分子而甲烷是非极性分子。 |
用价层电子对互斥理论预测H2S和BF3的立体结构,两个结论都正确的是( )
| A.直线形;三角锥型 | B.V形;三角锥型 |
| C.直线形;平面三角形 | D.V形;平面三角形 |
下列说法不正确的是 ( )
| A.σ键比π键重叠程度大形成的共价键强 |
| B.两原子形成共价键时最多有一个σ键 |
| C.气体单质中,一定有σ键,可能有π键 |
| D.N2分子中有一个σ键,2个π键 |