(8分)在2 L密闭容器内,800 ℃时反应2NO(g)+O2(g)  2NO2(g)(正反应为放热反应)体系中,n(NO)随时间的变化如下表:
2NO2(g)(正反应为放热反应)体系中,n(NO)随时间的变化如下表:
| 时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
| n(NO)(mol) |
0.020 |
0.010 |
0.008 |
0.007 |
0.007 |
0.007 |
(1)如图中表示NO2变化曲线的是 。用O2表示从0 s~2 内该反应的平均速率v= mol/(L·s)。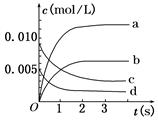
(2)能说明该反应已达到平衡状态的是 .
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v(NO)逆=2v(O2)正 d.容器内密度保持不变
(3)能使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
(14分)X、Y、Z、W是元素周期表中前四周期的常见元素,其相关信息如下表;
| 元素 |
相关信息 |
| X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y |
原子最外层电子数是次外层的三倍 |
| Z |
单质及其化合物的焰色反应为黄色 |
| W |
W元素基态原子的M层全充满,N层只有一个电子 |
⑴ X位于元素周期表第族 。X的一种单质熔点很高,硬度很大,则这种单质的晶体属于晶体。
。X的一种单质熔点很高,硬度很大,则这种单质的晶体属于晶体。
⑵ X与Y中电负性较强的是(填元素符号);XY2的电子式是,分子中存在个σ键。
⑶Z2Y2中含有的化学键类型有。阴、阳离子的个数比为。
⑷W的基态原子核外电子排布式是。
⑸废旧印刷电路板上有W的单质A。用H2O2和H2SO4的混合溶液可溶出印刷电路板上的A。已知:
A(s)+H2SO4(aq) ="=" ASO4(aq) + H2(g) ΔH=+64.4kJ·mol-1
2H2O2(l) ="=" 2H2O(l) + O2(g) ΔH= -196.4kJ·mol-1
H2(g)+ O2(g) ="=" H2O(l) ΔH= -285.8kJ·mol-1
O2(g) ="=" H2O(l) ΔH= -285.8kJ·mol-1
请写出A与H2SO4、H2O2反应生成ASO4(aq)和H2O(l)的热化学方程式(A用化学式表示):
。
有一包白色固体粉末,可能含有Na2SO4,CaCO3,KCl,BaCl2,CuSO4中的一种或几种,按以下步骤进行实验:
1.将固体粉末溶于水得到无色溶液和白色沉淀;
2.加以足量的稀盐酸,沉淀部分溶解且有气泡产生。
根据以上实验产生的现象,判断这混合物里,一定含有物质。一定没有
物质,可能含有的物质。
写出1的反应方程式
写出2的反应方程式
用CuSO4·5H2O配制500mL0.2 mol·L-1CuSO4溶液,在下列空格中填写所用仪器的名称及操作方法:
(1)经计算需要CuSO4·5H2O:克;
(2)把CuSO4·5H2O放入烧杯中,加入适量水溶解;
(3)把所得溶液沿玻璃棒注入容积为的中,并用适量水洗涤
和2~3次,把洗涤液也移入容量瓶中,并摇匀;
(4)再缓缓地加水,到接近刻度线1cm~2cm处,改用加水,使溶液的凹液面的最低处与刻度线相切;
下图所示装置在中学化学实验中常用物质的分离与提纯
(1)仪器甲的名称是
(2)上图存在一处错误,请指出存在错误的区域
(3)图中错误改正后,该装置可完成下列那个实验
A.除去CO2气体中混有的少量HCl气体
B.从硝酸钾和氯化钠的混合物提取硝酸钾
C.用含有Fe3+的自来水获得少量纯净的水
元素及其化合物的知识是“化学I”的重点内容。 A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如下图所示: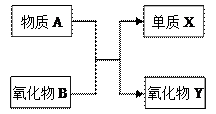
试写出符合下列条件的化学方程式:
(1)若物质A为氧化物: ;
(2)若A为金属单质,B为金属氧化物: ;
(3)若A为金属单质,B为非金属氧化物: ;
(4)若A和X均为非金属单质: ;