某有机物其结构简式如图所示,关于该有机物下列叙述不正确的是 ( )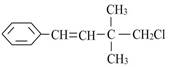
| A.能与NaOH的醇溶液共热发生消去反应 |
| B.能使溴水褪色 |
| C.一定条件下,能发生加聚反应 |
| D.一定条件下,能发生取代反应 |
下列各种变化中,不属于化学变化的是
| A.加热胆矾得到白色的无水硫酸铜粉末 |
| B.向鸡蛋溶液中滴入饱和硫酸钠溶液,析出白色沉淀 |
| C.向沸水中滴入饱和氯化铁溶液,制取氢氧化铁胶体 |
| D.向鸡蛋白溶液中滴入硝酸铅溶液,析出白色沉淀 |
某合作学习小组讨论辨析:①漂白粉和酸雨都是混合物;②煤和石油都是可再生能源;③不锈钢和目前流通的硬币都是合金;④硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物;⑤蛋白质溶液、淀粉溶液和雾都是胶体。上述说法正确的是
| A.①③⑤ | B.①②④ | C.②③④ | D.③④⑤ |
(12分)小明为验证NO2的氧化性和NO的还原性,设计了如下装置制取NO2和NO,并验证其性质,装置图如下: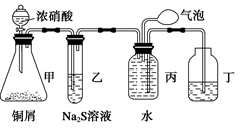
(1)写出甲中反应的离子方程式___________________________________________,乙中的现象是_______________________________,可证明NO2的氧化性;在丙中鼓入空气后现象是,可证明NO的还原性。
(2)实验前丙中充满水的作用是_________________________________________。
(3)小华对小明的实验设计提出了质疑,他认为乙中的现象不足以证明NO2的氧化性,他的理由是。
你认为怎样才能准确证明NO2的氧化性?(简要回答出原理和现象即可)_______________________________________________________________________ 。
将质量相等的铜片和铂片插入硫酸铜溶液中,铜片与电源正极相连,铂片与电源负极相连,以电流强度1A通电10min,然后反接电源,以电流强度2A继续通电10min。下列表示铜电极、铂电极、电解池中产生气体的质量和电解时间的关系图正确的是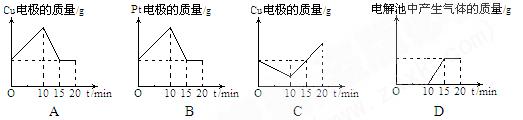

同温同压下,下列各组热化学方程式中,满足Q2>Q1的是
| A.2H2(g) + O2(g) = 2H2O(g);△H =-Q1 2H2(g) + O2(g) = 2H2O(l);△H =-Q2 |
| B.S(g)+O2(g)=SO2(g);△H =-Q1 S(s)+O2(g)=SO2(g);△H =-Q2 |
| C.C(s)+1/2O2(g)=CO(g); △H =-Q1 C(s)+O2(g)=CO2(g); △H =-Q2 |
| D.H2(g)+Cl2(g)=2HCl(g);△H =-Q11/2H2(g)+1/2Cl2(g)=HCl(g);△H =-Q2 |