元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z基态原子的2p轨道上有3个未成对电子。下列说法正确的是
| A.X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有12mol σ键 |
| B.Z的最高价含氧酸分子中,羟基氧和非羟基氧个数比为1:1 |
| C.Y的气态氢化物分子中H—Y—H键角比Y的最高价氧化物分子中O—Y—O键角小 |
| D.Z的气态氢化物比Y的气态氢化物稳定,是因为氢键的影响 |
关于下列各装置图的叙述中,不正确的是
| A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 |
| B.装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+ |
| C.装置③中钢闸门应与外接电源的负极相连 |
| D.装置④中的铁钉几乎没被腐蚀 |
下列说法正确的是()
| A.热化学方程式中,如没有注明温度和压强,表示反应热是在标准状况下测得的数据 |
| B.升高温度和增加反应物的浓度,都使反应物活化分子数和活化分子百分数同时增加 |
| C.化学反应速率可通过实验测定,比如可以测量在一定温度和压强下释放出来的气体的体积,或者可以用比色的方法测定溶液颜色的深浅进行换算 |
| D.物质发生化学变化不一定伴随着能量变化 |
常温下,分别将四块形状相同,质量为7 g的铁块同时投入下列四种溶液中,生成氢气速率最快的是
| A.200 mL 2 mol·L-1HCl | B.100 mL 2 mol·L-1H2SO4 |
| C.100 mL 3 mol·L-1HNO3 | D.50 mL 18.4 mol·L-1H2SO4 |
如图所示,△H1="-393.5kJ/mol," △H2=-395.4kJ/mol,下列说法或表示式正确的是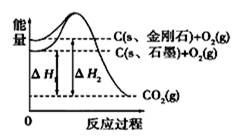
| A.石墨和金刚石的转化是物理变化 |
| B.C(s、石墨)=C(s、金刚石) △H="+1.9" kJ/mol |
| C.金刚石的稳定性强于石墨 |
| D.断裂1mol石墨化学键吸收的能量比断裂1mol金刚石的化学键吸收的能量少 |
将等质量的两份锌a、b分别加入过量的稀硫酸,同时向a中加少量的CuSO4溶液,下图中产生氢气的体积V(L)与时间t(min)的关系,其中正确的是()