下列物质存放方法错误的是
| A.铝片长期放置在不密封的纸盒里 |
| B.漂白粉长期放置在烧杯中 |
| C.FeSO4溶液存放在加有少量铁粉的试剂瓶中 |
| D.金属钠存放于煤油中 |
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示。下列说法不正确的是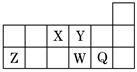
| A.元素的非金属性:Y>W |
| B.阴离子的还原性:W2->Q- |
| C.离子半径:Y2->Z3+ |
| D.Q、W、Y对应的氢化物的沸点逐渐降低 |
原电池产生电流的本质原因是
| A.原电池中电解质溶液能电离出自由移动的离子 |
| B.有两根导线将两个活动性不同的电极连接 |
| C.电极上进行的氧化还原反应的生成物为电子 |
| D.电极上进行氧化还原反应时有电子的定向移动 |
元素X原子的最外层有1个电子,元素Y原子的最外层有6个电子,这两种元素形成的化合物
| A.只能是离子化合物X2Y |
| B.只能是共价化合物X2Y2 |
| C.既可能是离子化合物也可能是共价化合物 |
| D.形成的化合物无论是X2Y还是X2Y2原子都达到了8电子稳定结构 |
市场上热销的富硒茶叶有很好的保健功能。硒的原子序数为 34,下列说法中正确的是
| A.硒元素的非金属性比溴元素的弱 |
| B.硒的最高价氧化物的水化物的分子式为:H2SeO3 |
| C.硒在周期表中位于第五周期VIA族 |
| D.硒的气态氢化物的稳定性比硫化氢强 |
根据下表中所列键能(形成或断开1mol化学键所放出或吸收的能量)数据,判断下列分子中最稳定的分子是
| 化学键 |
H—H |
H—Cl |
H—I |
Cl—Cl |
Br—Br |
| 键能(kJ/mol) |
436 |
431 |
299 |
247 |
193 |
A.HCl B.HBr C.H2 D.Br2