(10分)原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物最多的元素之一,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29。
回答下列问题:
(1)写出元素名称:X 、Y 。
(2)Y2X2分子中Y原子轨道的杂化类型为 ,1mol Y2X2含有σ键的数目为 。
(3)化合物ZX3中Z原子轨道的杂化类型为 ,ZX3的沸点比化合物YX4的高,其主要原因是 。
(4)元素Y的一种氧化物与元素Z的一种氧化物互为等电子体,元素Z的这种氧化 物的分子式是 。
(5)元素W的一种氯化物晶体的晶胞结构如图所示,该氯化物的化学式是 ,它可与浓盐酸发生非氧化还原反应,生成配合物H nWCl3,反应的化学方程式为 。
.有甲、乙、丙三种物质: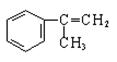
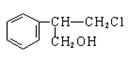

甲乙丙
(1)乙中含有的官能团的名称为____________________。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):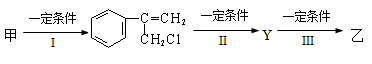
其中反应I的反应类型是_________,反应II的条件是_______________,反应III的化学方程式为__________________________________(不需注明反应条件)。
(3)由甲出发合成丙的路线之一如下: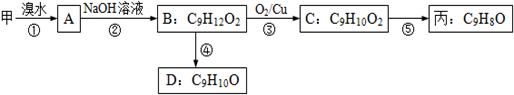
(a)下列物质不能与B反应的是(选填序号)。
a.金属钠 b.FeCl3c.碳酸钠溶液 d.HBr
(b)丙的结构简式为。
(c)任写一种能同时满足下列条件的D的同分异构体结构简式。
a.苯环上的一氯代物有两种
b.遇FeCl3溶液发生显色反应
c.能与Br2/CCl4发生加成反应
(10分)根据下面各物质之间的转化关系,回答问题: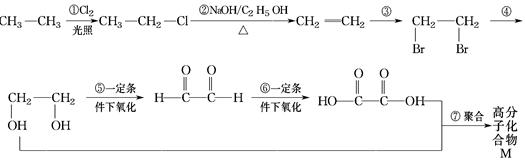
(1)属于取代反应的有(填序号,下同)___________,属于加成反应的有 _________。
(2)写出反应③、④的化学方程式(有机物用结构简式表示,注明反应条件,下同)
a.反应③___________________________________________________________。
b.反应④__________________________________________________________。
(3)写出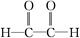 和新制氢氧化铜悬浊液(NaOH碱性环境)反应的化学方程式
和新制氢氧化铜悬浊液(NaOH碱性环境)反应的化学方程式
___________________________________________________________________。
(4分)取14.3gNa2CO3•XH2O溶于水配成100mL溶液,然后逐滴滴入稀盐酸直至没有气体放出为止,用去盐酸20.0mL,并收集到1.12LCO2(标准状况)。试计算:
(1)稀盐酸物质的量浓度为 mol/L;
(2)x值是。
(4分)拆开1mol气态物质中某种共价键需要吸收的能量,就是该共价键的键能。下表是某些共价键的键能:
| 共价键 |
H-H |
O=O |
H-O |
| 键能/kJ ·mol-1 |
436 |
498 |
X |
根据下图中能量变化图,回答下列问题: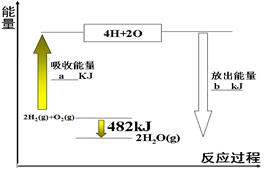
(1) 图中:a=___________。
(2) 表格中:X=。
(4分)(1)写出下列物质的化学式:①漂白粉的有效成分:;②钡餐:。
(2)写出用Na2SO3与浓H2SO4反应制备SO2的化学方程式:。