在下列各溶液中,离子一定能大量共存的是

A.强碱性溶液中:K+、Al3+、Cl-、SO42- |
B.含有0.1 mol·L-1 Fe3+的溶液中:K+、Mg2+、I-、NO3- |
C.含有0.1 mol·L-1Ca2+溶液在中:Na+、K+、CO32-、Cl- |
D.室温下,pH=1的溶液中: Na+、Fe3+、NO3-、SO42- |
能正确表示下列反应的例子方程式是
| A.向次氯酸钙溶液通入过量CO2:Ca2++2ClO—+CO2+H2O =CaCO3↓+2HClO |
| B.向次氯酸钙溶液通入SO2:Ca2++2ClO—+SO2+H2O= CaSO3↓+2HClO |
| C.氢氧化钙溶液与碳酸氢镁溶液反应:HCO3—+Ca2++OH—=CaCO3↓+H2O |
| D.在氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO3—=3Fe3++NO↑+2H2O |
Fe(OH)3胶体和MgCl2溶液共同具有的性质有
| A.都比较稳定,密封放置不产生沉淀 | B.两分散系均有丁达尔现象 |
| C.加入盐酸先产生沉淀,随后溶解 | D.分散质微粒可通过半透膜 |
将标准状况下的a升氨气溶于1000克水中,得到的氨水的密度为b克/毫升,则该氨水的物质的量的浓度是
A.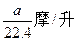 |
B.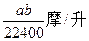 |
C.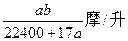 |
D. |
已知25%氨水的密度为0.91克/厘米3,5%氨水的密度为0.98克/厘米3,若将上述两溶液等体积混合,所得氨水溶液的质量分数是
| A.等于15% | B.大于15% | C.小于15% | D.无法估算 |