根据下图中所示装置回答下列问题。

A B C D E、
(1)图中仪器a的名称,
(2)用大理石和稀盐酸制取二氧化碳时,可选用的发生装置和收集装置是(填字母,下同),并写出此反应的化学方程式。
(3)用高锰酸钾制取氧气时,装置A还需要做的一点改动是。要收集一瓶较纯净的氧气应选用的装置是。
(4)实验室制取氢气可选用的发生装置和收集装置是。
化学与生活、生产息息相关,根据所学知识回答下列问题:
(1)随意丢弃塑料会造成“白色污染”,塑料不属于 (填选项);
A.有机物 B.合成材料 C.纯净物
(2)能使硬水软化的方法是 (填选项)
A.加入明矾 B.加入活性炭 C.煮沸
(3)铁制品表面涂一层油漆能防锈蚀,其原理是阻止了铁与 接触;
(4)碳酸氢钠是治疗胃酸过多症的一种药剂,它与盐酸反应的化学方程式为 。
(5)医用生理盐水中含有一定量的氯离子,请画出Cl﹣的离子结构示意图 。
用化学用语填空:
(1)2个汞原子 ,
(2)3个铁离子 ,
(3)4个氨分子 ,
(4)加碘盐KIO3中I元素的化合价 ,
(5)核电荷数分别为8、12的两种元素所形成的化合物 ,
(6)绿色植物光合作用产生的单质 。
某化学兴趣小组对酸、碱、盐的部分性质进行探究。
[探究一]氢氧化钠与二氧化碳反应
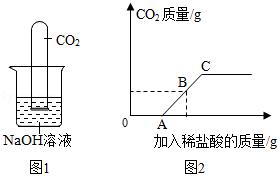
甲同学设计实验方案如图1所示
(1)实验现象为 ,甲同学由此判断氢氧化钠和二氧化碳发生了反应。
(2)小组内其他同学认为甲同学方案不完善,理由是 。
[探究二]氢氧化钠和盐酸发生中和反应时放出热量。
乙同学向一定量10%的氢氧化钠溶液中滴加10%的盐酸,滴加过程中温度变化如表
|
加入盐酸体积V/mL |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
16 |
18 |
20 |
|
混合溶液温度 T/℃ |
15.2 |
19.6 |
22.0 |
26.0 |
28.2 |
26.7 |
25.7 |
24.7 |
23.7 |
22.9 |
(3)反应的化学方程式为 。
(4)根据表中数据分析混合溶液温度变化的原因 。
(5)小组内其他同学提出“将10%的盐酸直接滴入氢氧化钠固体中也能得出相同结论”,你认为是否合理并说明理由 。
(6)丙同学将甲同学和乙同学实验后的溶液混合,未发现明显现象。现将混合液中的氯化钠进行提纯,具体的操作为 。
[探究三]碳酸钠溶液与稀盐酸的分步反应
[查阅资料]向碳酸钠溶液中逐滴加入稀盐酸的反应是分步反应,第一步反应生成碳酸氢钠和氯化钠,当碳酸钠反应完后才发生第二步反应。
丁同学向106g质量分数为10%的碳酸钠溶液中逐滴加入质量分数为3.65%的稀盐酸,生成二氧化碳的质量变化如图2所示(不考虑CO2的溶解)。
(7)A→C段发生反应的化学方程式为 。
(8)若B点横坐标为150,则其纵坐标为 。
人类社会发展离不开金属材料。如图是某硬铝的主要成分。
(1)硬铝属于 (填“合金”或“纯金属”)。
(2)将适量硬铝(已砂纸打磨处理)放入足量稀硫酸中,观察到现象为 ,反应的化学方程式有 。
(3)将足量硬铝粉末放入硝酸银溶液中,充分反应后,溶液出现蓝色,出现蓝色的原因是 ,写出此时溶液中溶质成分并说明理由 。

学会物质的分离提纯和准确配制一定质量分数的溶液在实际应用中有重要意义。
(已知:20℃氯化钠的溶解度为36g,水的密度可近似看作1g/mL)
实验一:溶液配制
(1)用氯化钠固体配制100g质量分数为5%的氯化钠溶液。需要氯化钠 g,水 mL。
(2)0.9%的医用氯化钠溶液俗称生理盐水,可用于补充人体所需电解质。生理盐水中的溶质为 。
实验二:粗盐提纯

(3)操作①中玻璃棒的作用是 ,操作②的名称为 。
(4)20℃时提纯9g粗盐,若已知粗盐中氯化钠含量约为80%,溶解时应选择哪一种规格的量筒量取所需要的水最为合适(提供的量筒规格有“10mL“”、“25mL”和“100mL”),请你选择并说明理由 。
(5)提纯后的精盐属于 (填“纯净物”或“混合物”)。