某化学兴趣小组的同学在整理学校实验时,发现了一瓶标签中化学式已破损(如图所示)但未变质的无色溶液,他们对这瓶无色溶液产生了兴趣.经过询问实验老师得知,这瓶无色溶液的溶质应该是碳酸钠、氯化钠、硫酸钠、氢氧化钠中的一种.请你与他们一起对这瓶溶液的溶质成分进行探究.
【提出问题】这瓶无色溶液溶质成分是什么?
【提出假设】①碳酸钠(
)②硫酸钠(
)③氯化钠(
)④氢氧化钠(
)
【查阅资料】硫酸钠、氯化钠的溶液呈中性,碳酸钠、氢氧化钠的溶液呈碱性.
【讨论交流】为了确定该瓶溶液溶质的成分,首先他们根据标签上物质元素组成的特点,认为该瓶溶液不可能是
【实验探究】
| 实验操作 |
实验现象 |
| 取少量样品溶液于试管中,滴加稀盐酸 |
产生大理气泡 |
【实验结论】通过对上述实验现象的分析,你认为假设
【反思拓展】通过上述【讨论交流后】后,排除了四种假设物质中的两种.请你根据查阅资料所获取的知识,再举一例判定两种假设物质的实验方法

某小组同学探究二氧化碳(CO2)、氨气(NH3)分别与水反应后产物的酸碱性。他们收集了若干瓶CO2和NH3。
【确定标准】
老师指导该小组同学用自制的紫色石蕊试纸完成了如上图所示实验,确定检验酸碱性物质存在的标准。取三个洁净的表面皿,分别放上紫色石蕊试纸,向试纸上依次滴加稀盐酸、蒸馏水、氢氧化钠(碱)溶液,观察到三条试纸的颜色依次为红色、紫色和蓝色。
【实验过程】
(1)探究CO2与水反应产物的酸碱性。该小组同学向一瓶CO2中加入30 mL水,充分振荡。再取一个洁净的表面皿,放上一条紫色石蕊试纸,向试纸上滴加瓶中的液体,观察到紫色石蕊试纸变成红色,由此获得结论:瓶中液体里含有 性物质,发生反应的化学方程式为 。
(2)探究NH3与水反应产物的酸碱性。该小组同学用(1)的方法继续进行NH3的实验,他们分析液体里含有碱性物质,观察到的现象是 ,分析依据是 。
【实验反思】
有同学提出:仅用上述实验还不足以说明CO2或NH3与水发生了反应,还需补充一个对比实验,以NH3为例,该对比实验的操作为 ,观察到的现象为 。
化学兴趣小组同学对“铁生锈的条件”进行实验探究。
【进行实验】
| 实验 |
实验操作 |
实验现象 |
实验结论 |
| 1 |
 AB |
一段时间后, A中铁丝表面有红色固体生成 B中铁丝无明显变化 |
|
| 2 |
 CD |
一段时间后, C中 D中铁丝无明显变化 |
铁生锈需要与O2接触 |
某同学在家中发现,炒完菜的铁锅表面容易生锈。
【猜想与假设】可能是食盐对铁生锈的速率产生了影响。
【进行实验】该小组用实验装置E、F同时进行实验。其中集气瓶的容积相同,量筒内盛有等体积的水,F中集气瓶内另加入了某种物质。
| 实验装置 |
实验过程 |
实验结论 |
  E F |
一段时间后,打开止水夹,记录实验过程中量筒内剩余水的体积(每次测量时间间隔不等,实验数据见下表)。E中铁丝和F中另加入的物质表面均出现红色物质。 |
食盐可以加速铁的生锈 |
实验记录表
| 次数 |
1 |
2 |
3 |
4 |
5 |
6 |
|
| 量筒中剩余水的体积/mL |
E |
68 |
57 |
44 |
30 |
30 |
30 |
| F |
71 |
65 |
56 |
a |
30 |
30 |
(1)实验装置F中,集气瓶内另加入的物质是 。
(2)实验记录表中,a的取值范围是 。
【反思与应用】结合上述实验,谈谈你对家中铁锅使用的建议: 。
利用下图装置进行实验。
| 实验装置 |
实验过程 |
| 【实验1】探究可燃物燃烧的条件 ① 在A、B中各放一小块白磷(着火点为40℃),A中加入约1/3试管的80℃水,A、B中白磷均不燃烧; ② 从a处通入O2使A中热水恰好完全进入B中,A中白磷燃烧,B中白磷不燃烧; ③ ,B中白磷燃烧。 |
|
| 【实验2】探究MnO2在H2O2分解中的作用 ① A中加入约1/3试管的H2O2溶液,B中放入一面粘有MnO2的玻璃片,A、B中均无明显现象; ② 从c处抽气,使A中液体进入B中,观察到玻璃片上粘有MnO2的一面产生大量气泡,另一面无明显变化。 |
回答下列问题:
(1)实验1:步骤③中的操作是 。能说明“可燃物燃烧需要温度达到着火点”的实验现象是 。
(2)实验2:B中反应的化学方程式是 。该实验能否得出“MnO2是H2O2分解的催化剂”的结论?你的判断及理由是 。
用图装置探究相关问题: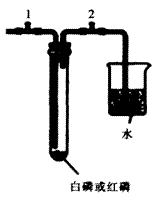
(1)检验装置的气密性。连接装置,关闭弹簧夹l、打开弹簧夹2。用酒精灯稍加热试管后,移去酒精灯,观察到现象:______________,说明装置气密性良好。
(2)取两套相同的装置,分别往试管中加入足量白磷、红磷后,连接仪器,关闭所有弹簧夹,再将两支试管同时放入同一热水中,观察到白磷燃烧,而红磷没有燃烧。可得到结论:
(3)试管中白磷燃烧一段时间后熄灭。撤去热水,仍关闭弹簧夹,待温度恢复到室温,打开弹簧夹2,可观察到的现象:让剩余白磷在水中继续燃烧的方法:
(4)请用该装置设计实验,探究影响燃烧剧烈程度的因素(其他用品自选)。
你的猜想:影响燃烧剧烈程度的一种因素是___________________。
实验设计(要求:写出操作步骤,描述控制变量具体方案):__________________
同学们对实验“煅烧石灰石”展开了探究。资料:石灰石中的杂质高温不分解且不与稀盐酸反应
①为证明石灰石已分解,三位同学设计方案如下:
I.甲同学按图一所示进行实验(煤气灯能达到石灰石分解的温度),观察到烧杯内壁石灰水变浑浊,写出石灰水发生反应的化学方程式(1) 。
II.乙同学按图二所示进行实验,观察到B中液体变(2) 色,A实验的作用(3) 。
III.丙同学取一定质量的石灰石煅烧,一段时间后发现固体质量减轻,证明石灰石已分解。
你认为哪位同学的方案不合理?并写出理由(4) 。
②为证明石灰石是否完全分解?丁同学对丙同学煅烧后的固体又进行了如下探究
| 实验步骤 |
实验现象 |
结论 |
| (5) |
有气泡产生 |
石灰石未完全分解 |