下表为部分短周期元素化合价及其相应原子半径的数据。下列说法正确的是
| 元素性质 |
元素编号 |
|||||||
| A |
B |
C |
D |
E |
F |
G |
H |
|
| 原子半径(nm) |
0.102 |
0.117 |
0.074 |
0.110 |
0.071 |
0.075 |
0.077 |
0.099 |
| 最高化合价 |
+6 |
+4 |
|
+5 |
|
+5 |
+4 |
+7 |
| 最低化合价 |
-2 |
-4 |
-2 |
-3 |
-1 |
-3 |
-4 |
-1 |
A.C为硫元素
B.A、B是同周期元素
C.F、H的简单离子的电子层结构相同
D.元素G在周期中的位置是第二周期第Ⅳ族
下列关于SO2的说法中,不正确的是( )
| A.SO2可使石蕊试液褪色 | B.SO2有漂白和杀菌作用 |
| C.SO2溶于水后生成H2SO | D.SO2是一种大气污染物 |
A(盐)和B(酸)反应,可放出有气味的气体C,C跟KOH反应又得到A(盐),C氧化的最终产物为W气,W气溶于水又得到B(酸)是( )
| A.K2S和稀H2SO4 | B.K2SO3和盐酸 |
| C.K2S和盐酸 | D.K2SO3和稀H2SO4 |
下列溶液露置于空气中,开始一段时间其pH变小的是(不考虑溶质挥发)( )
①H2O2②H2SO3③Na2S④Ca(OH)2⑤氯水⑥Na2SO3
| A.①②④ | B.②⑤⑥ |
| C.①②④⑤ | D.②④⑤⑥ |
下列离子方程式正确的是( )
A.二氧化硫通入足量KOH溶液中SO2+2OH-  +H2O +H2O |
B.往澄清石灰水中通入足量二氧化硫SO2+Ca2++2OH- CaSO3↓+H2O CaSO3↓+H2O |
C.往二氧化硫的水溶液中滴加少量NaOH溶液H2SO3+OH-  +H2O +H2O |
D.亚硫酸中滴加双氧水生成硫酸H2SO3+2H++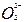  2H++ 2H++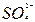 +2H2O +2H2O |
在氯化钡溶液通入SO2,溶液仍澄清,若将氯化钡溶液分装两支试管,一支加硝酸,另一支加NaOH溶液,然后再通入SO2,结果两试管中都有白色沉淀生成,由此得出下列结论合理的是( )
| A.氯化钡有两性 |
| B.两支试管中的白色沉淀都是BaSO4 |
| C.SO2具有还原性和酸性 |
D.加碱后溶液中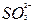 浓度增大 浓度增大 |