浙江大学的科研小组成功研制出能在“数分钟之内”将电量充满的锂电池,其成本只有传统锂电池的一半。他们把锂锰氧化物(LMO)浸泡在石墨里面,使其变成一个可以导电的密集网络的负极材料(如图),与电解质和正极材料(石墨)
构成可充电电池。若电解液为LiAlCl4-SOCl2,电池的总反应为:
4LiCl+S+SO2  4Li+2SOCl2。下列说法正确的是( )
4Li+2SOCl2。下列说法正确的是( )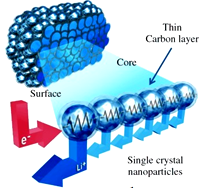
| A.电池的电解液可为LiCl水溶液 |
| B.该电池放电时,负极发生还原反应 |
| C.充电时阳极反应式为:4Cl-+S+SO2-4e-=2SOCl2 |
| D.放电时电子从负极经外电路流向正极,再从正极经电解质流向负极 |
在金属晶体中,自由电子与金属离子的碰撞中有能量传递,可以用此来解释的金属的物理性质是
| A.延展性 | B.导电性 | C.导热性 | D.硬度 |
在10mL0.1mol·L-NaOH溶液中加入同体积、同浓度的HAc溶液,反应后溶液中各微粒的浓度关系错误的是
A C(Na+)>C(Ac-)>C(H+)>C(OH-) B C(Na+)>C(Ac-)>C(OH-)>C(H+)
C C(Na+)=C(Ac-)>C(HAc) D C(Na+)+C(H+)=C(Ac-)+C(OH-)
在常温下10mL pH=10的KOH溶液中,加人pH=4的一元酸HA溶液至pH刚好等于7(假设反应前后体积不变),则对反应后溶液的叙述正确的是
| A.c(A-)=c(K+) | B.c(H+)=c(OH-)<c(K+)<c(A-) |
| C.V总≥20mL | D.V总≤20mL |
常温下把盐酸和氨水等体积混合后,其溶液的PH值恰好等于7,则下列说法正确的是 ( )
| A.盐酸中C(H+)一定大于氨水中C(OH-) |
| B.盐酸的物质的量浓度一定小于氨水的物质的量浓度 |
| C.反应后生成的盐溶液没有发生水解 |
| D.盐酸中氯化氢的物质的量等于氨水中氨的物质的量 |
下列溶液中各微粒的浓度关系不正确的是
| A.0.1 mol·L-1 HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+) |
| B.1 L 0.l mol·L-1CuSO4·(NH4)2SO4·6H2O的溶液中: c(SO42-)>c(NH4+) >c(Cu2+)>c(H+)>c(OH-) |
| C.0.1 mol·L-1NaHCO3溶液中: c(Na+)+c(H+) =c(HCO3-)+c(CO32-)+c(OH-) |
| D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中: |
c(Na+)>c(HX)>c(X-)>c(H+)>(OH-)