将11. 2L标准状况下的甲烷和乙烯的混合气体通入足量的溴的四氯化碳溶液中充分反应,溴的四氯化碳溶液增加了5.6g,求原混合气体中甲烷与乙烯的质量之比。
1774年,瑞典化学家舍勒发现软锰矿(主要成分是MnO2)和浓盐酸混合加热能制取氯气:
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
现将含MnO2的质量为17.4g的软锰矿石与足量浓盐酸完全反应(杂质不参加反应)。计算:
(1)生成的Cl2的体积(标准状况)。
(2)参加反应的HCl的物质的量。
向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH的混合溶液B,产生的沉淀总物质的量和加入溶液B的体积关系如图所示: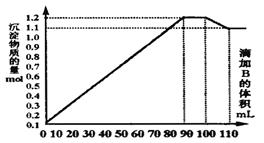
(1)当加入B溶液110 mL时,溶液中的沉淀是(填化学式)
(2)将A.B溶液中各溶质的物质的量浓度填入下表:
| 溶质 |
Na2SO4 |
BaCl2 |
AlCl3 |
FeCl3 |
| /mol·L-1 |
(3)写出滴加B溶液90-100mL时的离子方程式:
。
硝酸与金属反应时,浓度越稀还原产物价态越低。现用一定量的铝粉与镁粉组成的混合物与100ml硝酸钾 溶液与硫酸组成的混合溶液充分反应,反应过程中无任何气体放出,相反应后的溶液中逐滴加入4.00mol/L的NaOH溶液,加入的溶液体积与与产生的沉淀质量的关系如图所示。
溶液与硫酸组成的混合溶液充分反应,反应过程中无任何气体放出,相反应后的溶液中逐滴加入4.00mol/L的NaOH溶液,加入的溶液体积与与产生的沉淀质量的关系如图所示。
回答下列问题:
(1)写出铝与混合溶液反应的离子方程式:
(2)参加反应硝酸根离子物质的量为mol
(3)参加反应的铝与镁的质量比为
(4混合液中硫酸的物质的量的浓度为mol /L
/L
现有含碳酸钠杂质的氯化钠样品10克,与足量的盐酸反应,生成的气体在标准状况下体积为224mL,求:
(1)生成的气体是______________,物质的量为____________。
(2)该样品中含氯化钠的质量分数?(写出计算过程)
(共10分)常温下,将20.0g14.0%的NaCl溶液跟30.0g24.0%的NaCl溶液混合,得到密度为1.15g/cm3的混合溶液。求: (1)、该混合溶液的质量分数?
(1)、该混合溶液的质量分数?
(2)该混合溶液的物质的量浓度?
(3)在1000g水中溶解多少摩尔NaCl才能使其浓度与上述溶液的浓度相等?