反应A+3B=4C+2D,在不同条件下反应,其平均反应速率v(X)(表示反应物的消耗速率或生成物的生成速率)如下,其中反应速率最快的是
A.v(A)=0.4mol/(L·s) B.v(B)=0.8mol/(L·s)
C.v(C)=1.2mol/(L·s) D.v(D)=0.7mol/(L·s)
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s)下列说法中错误的是
| A.电池工作时,锌失去电子,锌是负极 |
| B.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
| C.电池正极的电极反应式为:2MnO2+H2O+2e—==Mn2O3+2OH— |
| D.电池工作时,溶液中OH-向正极移动,K+、H+向负极移动 |
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:
N2(g)+3H2(g)  2NH3(g),673 K,30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是( )
2NH3(g),673 K,30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是( ) 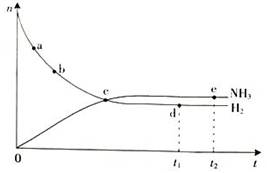
| A.点e的正反应速率比点d的大 |
| B.点c处反应达到平衡 |
| C.点d(t1时刻)和点e(t2时刻)处n(N2)相同 |
| D.在给定条件下,t1时刻NH3的含量达到最高 |
下列物质之间的相互关系不正确的是
A.O2和O3互为同素异形体B.
C.H、D、T互为同位素D.干冰和冰为不同一种物质
下列反应既属于氧化还原反应,又是吸热反应的是()
| A.铝片与盐酸的反应 | B.灼热的碳与CO2的反应 |
| C.Ba(OH)2·8H2O与NH4Cl的反应 | D.甲烷在氧气中的燃烧反应 |
下列说法中正确的是()
A.所有主族元素正化合价数,等于它的族序数
B.ⅦA族元素的原子随核电荷数的增加,得电子能力逐渐减弱
C.ⅠA、ⅡA族元素的阳离子与同周期稀有气体元素的原子具有相同的核外电子排布
D.前三周期元素中共有非金属元素12种