要使含有Ba2+、Al3+、Cu2+、Ag+等离子的溶液中的各离子逐一形成沉淀析出,下列所选择的试剂及加入试剂的顺序正确的是
| A.H2SO4—HCl—NaOH—CO2 | B.HCl—H2SO4—NaOH—CO2 |
| C.NaCl—Na2SO4—NaOH—CH3COOH | D.Na2SO4—NaCl—NaOH—HCl |
下列有关物质的性质或应用均正确的是
| A.工业上分别用电解氧化镁和氧化铝的方法制备镁和铝 |
| B.铁具有良好的导电性,氯碱工业中可用铁作阳极电解食盐水 |
| C.氢氧化镁分解时吸收大量的热量,添加到合成树脂中可作阻燃剂 |
| D.用二氧化硫加工银耳,使之更白 |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.1.0 mol/L的NaHSO4溶液:K+、Fe2+、NO3-、Cl- |
| B.l.0 mol·L-1 NaClO溶液:Fe2+、K+、I一、Cl- |
| C.甲基橙显黄色的溶液: Na+、CO32-、NO3-、SO32- |
| D.在c(H+)/c(OH-) = 1×1013的溶液:NH4+、Ca2+、C1-、K+ |
下列有关化学用语表述正确的是
| A.羟甲基(-CH2OH)和甲氧基(CH3O-)电子数不相等 |
B.S2-的结构示意图: |
C.质子数为53,中子数为78的碘原子: |
D.苯甲醛: |
随着社会的发展,人们日益重视环境问题、节能减排,下列说法不正确的是
| A.绿色化学的核心是利用化学原理从源头上减少和消除工农业生产等对环境的污染 |
| B.大力开发和应用氢能源有利于实现“低碳经济” |
| C.吸烟不会造成室内PM2.5污染 |
| D.采用催化转换技术将汽车尾气中的NOx和CO转化为无毒气体 |
海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案: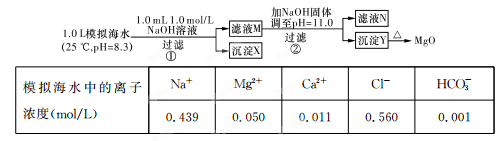
注:溶液中某种离子的浓度小于1.0×10-5 mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变。已知:KSp(CaCO3)=4.96×10-9;KSp(MgCO3)=6.82×10-6;KSp[Ca(OH)2]=4.68×10-6;KSp[Mg(OH)2]="5.61×10" -12。
下列说法不正确的是
| A.沉淀物X为CaCO3 |
| B.滤液M中存在Mg2+和Ca2+ |
| C.滤液N中存在Mg2+、Ca2+ |
| D.步骤②中若改为加入4.2 g NaOH固体,沉淀物Y只有Mg(OH)2 |