化学实验应与化工生产一样遵循绿色化学的原则,实现原料和过程绿色化。下列操作符合绿色化学原则的是
| A.为便于观察铜在氯气中燃烧的现象,加大氯气的使用量 |
| B.实验室改用H2O2和MnO2反应,代替加热KClO3和MnO2制取氧气 |
| C.焚烧塑料、橡胶等废弃物是处理城市生产、生活垃圾的有效方法 |
D.制取CuSO4: Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O CuSO4+SO2↑+2H2O |
某种氢氧燃料电池的电解液为KOH溶液。下列有关电池的叙述不正确的是
| A.负极反应式为:H2+2OH-—2e-==H2O |
| B.工作一段时间后,电解液中的KOH的物质的量不变 |
| C.该燃料电池的总反应方程式为:2H2+O2==2H2O |
| D.用该电池电解CuCl2溶液,产生2.24LCl2(标准状况)时,有0.1mol电子转移 |
下列有关金属腐蚀与防护的说法正确的是
| A.纯银器表面在空气中主要因电化学腐蚀渐渐变暗 |
| B.当镀锡铁制品的镀层破损时,镶层仍能对铁制品起保护作用 |
| C.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
| D.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
在一密闭烧瓶中,在25℃时存在如下平衡:2NO2(g)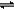 N2O4(g) △H<0,把烧瓶置于100℃的水中,则下列几项性质中不会改变的是:①颜色 ②平均相对分子质量 ③质量 ④压强 ⑤密度
N2O4(g) △H<0,把烧瓶置于100℃的水中,则下列几项性质中不会改变的是:①颜色 ②平均相对分子质量 ③质量 ④压强 ⑤密度
| A.①和③ | B.②和④ | C.③和⑤ | D.④和⑤ |
常温下,在pH=2的硫酸溶液中,水电离出来的H+的物质的量浓度为
| A.10-2 mol/L | B.10-12 mol/L | C.2×10-12 mol/L | D.0.02mol/L |
下列说法正确的是
| A.能够发生化学反应的碰撞是有效碰撞 | B.反应物分子的每次碰撞都能发生化学反应 |
| C.活化分子之间的碰撞一定是有效碰撞 | D.增大反应物浓度时,活化分子百分数增大 |