在一定温度下,反应A2(g)+B2(g)  2AB(g)达到反应限度的标志是
2AB(g)达到反应限度的标志是
A.容器内气体的总压强不随时间变化而变化
B.A2和B2物质的量之和与AB的物质的量相等
C.c(A2):c(B2):c(AB)=1:1:2
D.A2、B2和AB的物质的量不再改变
用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中,正确的是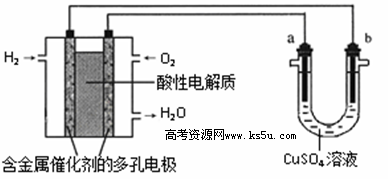
| A.燃料电池工作时,正极反应为:O2 + 2H2O + 4e-= 4OH- |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
下列关于电解质溶液的叙述正确的是
| A.常温下,同浓度的Na2CO3与NaHCO3溶液相比,Na2CO3溶液的pH大 |
| B.常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Clˉ)>c(NH4+)>c(H+)=c(OHˉ) |
| C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D.将pH = 4的盐酸稀释后,溶液中所有离子的浓度均降低 |
M的名称是乙烯雌酚,它是一种激素类药物,结构简式如下。下列叙述不正确的是
| A.M的分子式为C18H20O2 |
| B.M可与NaOH溶液或NaHCO3溶液均能反应 |
| C.1 mol M最多能与7 mol H2发生加成反应 |
| D.1 mol M与饱和溴水混合,最多消耗5 mol Br2 |
下列离子方程式中正确的是
| A.向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2+ + OH- + H+ + SO42-= BaSO4↓+ H2O |
B.NH4HCO3溶液与过量KOH浓溶液共热:NH4++ OH- NH3↑+ H2O NH3↑+ H2O |
| C.稀硝酸和过量的铁屑反应:3 Fe + 8H+ +2 NO3- =" 3" Fe3+ +2 NO↑ + 4 H2O |
| D.KI溶液与H2SO4酸化的H2O2溶液混合:2 I- + H2O2 + 2 H+ ="2" H2O + I2 |
短周期元素X、Y、Z,其中X、Y位于同一主族,Y、Z位于同一周期。X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比Y原子少1。下列比较正确的是
| A.元素非金属性:Z> Y > X | B.最高价氧化物水化物酸性:Z > Y |
| C.原子半径:Z < Y < X | D.气态氢化物的稳定性:Z < Y < X |