(原创)能用键能大小解释的是
| A.稀有气体一般很难发生化学反应 |
| B.常温常压下,氟气的密度小于氯气 |
| C.相同条件下,NH3在水中的溶解度大于PH3 |
| D.SiC晶体的熔点比晶体硅的高 |
已知NO2和N2O4可以相互转化:2NO2(g) N2O4(g) △H<0。在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化
N2O4(g) △H<0。在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化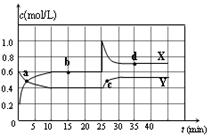
关系如右图。下列说法正确的是
| A.图中的两条曲线,X是表示NO2浓度随时间的变化曲线 |
| B.前10 min内用v(NO2)表示的化学反应速率为0.06 mol/(L·min) |
| C.25 min时,导致平衡移动的原因是将密闭容器的体积缩小为1L |
| D.a、b、c、d四个点中,只有b、d点的化学反应处于平衡状态 |
常温下的下列情况中,一定能大量共存于同一溶液中的离子组是
| A.使甲基橙呈红色的溶液中:I-、Cl-、NO3-、Na+ |
| B.使石蕊呈蓝色的溶液中:NH4+、Al3+、NO3-、HCO3- |
| C.由水电离出的c(H+)=1×10 -12mol·L -1的溶液中:K+、Cl-、NO3-、Na+ |
| D.含有大量Al3+的溶液中:K+、Mg2+、Na+、ClO- |
下列叙述中,不正确的是
| A.在相同条件下,焓变小于0而熵变大于0的反应肯定能自发进行 |
| B.升高温度会加快化学反应速率,其原因是增加了活化分子的百分数 |
| C.青石棉的化学式为Na2Fe5Si8O22(OH)2,用氧化物的形式可表示为: Na2O·3FeO·Fe2O3·8SiO2·H2O |
| D.某离子被沉淀完全时,该离子在溶液中的浓度即为0 |
大胆、科学的假设与猜想是科学探究的先导和价值所在。在下列假设(猜想)引导下的探究肯定没有意义的是
| A.探究SO2和Na2O2反应可能有Na2SO4生成 |
| B.探究Na与水的反应可能有O2生成 |
| C.探究浓硫酸与铜在一定条件下反应产生的黑色物质中可能有CuS |
| D.探究向滴有酚酞试液的NaOH溶液中通以Cl2,酚酞红色褪去的现象是溶液的酸碱性改变所致,还是HClO的漂白性所致 |
下列反应的离子方程式正确的是
| A.Fe2O3溶于过量的氢碘酸中:Fe2O3+6H+=2Fe3++3H2O |
| B.向NaAlO2溶液中通入过量CO2: AlO2-+CO2+2H2O = Al(OH)3↓+ HCO3 |
| C.向漂白粉溶液中通入SO2气体:Ca2++2C1O-+SO2 +H2O= CaSO3↓+2H C1O |
| D.向Fe(NO3)2溶液中加入稀盐酸:3Fe2++4H++NO3-==3Fe3++NO↑+2H2O |