(9分)已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A 与其他4种元素既不在同一周期又不在同一主族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第7列元素。D的原子序数比E小5,D跟B可形成离子化合物其晶胞结构如右图。 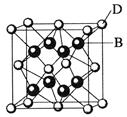
 (1)A的元素符号是 ;E在元素周期表中的位置是 ,它的+2价离子的电子排布式为 。
(1)A的元素符号是 ;E在元素周期表中的位置是 ,它的+2价离子的电子排布式为 。  (2)B的氢化物的晶体类型是 晶体,B的氢化物与C的氢化物相比,分子极性较大的是 (写化学式)。
(2)B的氢化物的晶体类型是 晶体,B的氢化物与C的氢化物相比,分子极性较大的是 (写化学式)。 (3)从图中可以看出,D跟B形成的离子化合物的电子式为 ;该离子化合物晶体的密度为ag·cm-3,则晶胞的体积是 (只要求列出算式)。
(3)从图中可以看出,D跟B形成的离子化合物的电子式为 ;该离子化合物晶体的密度为ag·cm-3,则晶胞的体积是 (只要求列出算式)。
阅读如下信息后完成问题:元素M是仅次于铁而在生物细胞中大量存在的金属元素,是人体必需元素之一;M用于制合金、白铁、干电池、烟火等;其粉末为强还原剂,可用于有机合成、染料制备以及金、银的冶炼;其氧化物是一种白色颜料。
(1)M的元素符号是_______________,核外电子数有_______________个。
(2)M的最重要的两种矿物的化学式是_______________和_______________。
(3)M的最重要的一种“矾”的名称是_______________,化学式是________________。
(4)M能否与强酸(HCl)或强碱(NaOH)反应。如果能,写出离子方程式。
实验室为监测空气中汞蒸气的含量,往往悬挂涂有CuI的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为:4CuI+Hg=Cu2HgI4+2Cu
(1)上述反应产物Cu2HgI4中,Cu元素显_______________价。
(2)以上反应中的氧化剂为_____________________,当有1 mol CuI参与反应时,转移电子_______________mol。
(3)CuI可由Cu2+与I-直接反应制得,请配平下列反应的离子方程式: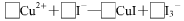
埋藏在地下的青铜器锈蚀过程可以表示为:
(1)青铜器锈蚀过程中的产物有__________________________________________________。
(2)青铜器出土后防止青铜器继续锈蚀的关键是____________________________________。
氢氧化铝与其他的氢氧化物不同,既能与酸反应生成盐和水,又能与碱反应生成盐和水,试用离子方程式表示它与酸和碱反应的原理。