在一定条件下,反应N2+3H2 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为:
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为:
| A.v(NH3)="0.1" mol/(L·min) | B.v(N2)="0.02" mol/(L·min) |
| C.v(H2)="0.015" mol/(L·min) | D.v(NH3)="0.17" mol/(L·min) |
有机物的种类繁多,但其命名是有规则的。下列有机物命名正确的是()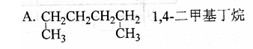
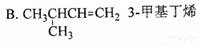
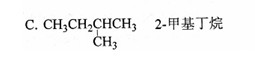
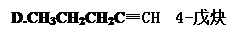
甲、乙两种非金属:①甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;②甲比乙更容易与氢气化合;③甲单质能与乙阴离子发生氧化还原反应;④与金属反应时,甲原子得电子数目比乙的多;⑤甲的单质熔沸点比乙的低。能说明甲比乙的非金属性强的是()
| A.①②③④ | B.①②③④⑤ | C.①②③ | D.②③④⑤ |
已知五种短周期元素的原子半径及主要化合价如下表:
| 元素代号 |
L |
M |
Q |
R |
T |
| 原子半径/nm |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
| 主要化合价 |
+2 |
+3 |
+6、-2 |
+2 |
-2 |
下列叙述不正确的是( )
A.L与Q形成的化合物属于离子化合物
B.T、Q的氢化物常温常压下均为无色气体
C.L、M的单质与稀盐酸反应速率:L > M
D.M与T形成的化合物具有两性
X、Y、Z三种主族元素,X+和Y-两种离子具有相同的电子层结构,Z原子核内质子数比Y原子核内质子数少9个,Y—在一定条件下可被氧化生成YZ3—。下列说法正确的是()
| A.YZ3—中的电子数为41 | B.化合物XYZ的溶液具有漂白性 |
| C.X、Y、Z均属于短周期元素 | D.Y属于第ⅤA族元素 |
下列关于原子结构、元素性质的说法正确的是()
| A.非金属元素组成的化合物中只含共价键 |
| B.235U与238U是中子数不同质子数相同的同种核素 |
| C.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数 |
| D.短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构 |