括号内物质为杂质,下列除去杂质的做法不正确的是
A.乙酸乙酯(乙酸和乙醇):用饱和Na2CO3溶液洗涤后分液 |
B.乙烷(乙烯):用浓溴水洗气 |
C.乙醇(乙酸):用NaOH溶液中和后分液 |
D.乙醇(水):用生石灰吸水后蒸馏 |
对于可逆反应M+N Q 达到平衡时,下列说法正确的是
Q 达到平衡时,下列说法正确的是
| A.M、N、Q三种物质的浓度一定相等 | B.M、N全部变成了Q |
| C.反应混合物各成分的百分组成不再变化 | D.反应已经停止 |
绿色化学对于化学反应提出了“原子经济性”(原子节约)的新概念及要求。理想的原子经济性反应是原料中的原子全部转变成所需产物。不产生副产物,实现零排放。下列反应中,原子经济性最好的是(反应均在一定条件下进行)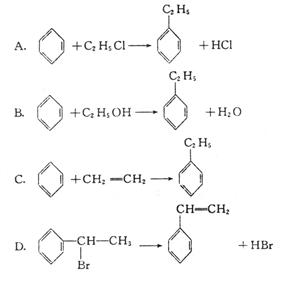
下列物质中含有共价键的离子化合物是
| A.NaOH | B.KCl | C.H2 O | D.H2 |
已知反应A+B=C+D的能量变化如图所示,下列说法正确的是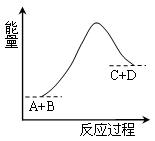
| A.该反应为放热反应 |
| B.该反应为吸热反应 |
| C.反应物的总能量高于生成物的总能量 |
| D.该反应只有在加热条件下才能进行 |