A、B、C为短周期元素,在周期表中所处的位置如图所示。A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等。
| A |
|
C |
| |
B |
|
(1)A、B、C三种元素的名称分别为 、 、 。
(2)B位于元素周期表中第 周期、第 族。
(3)C的原子结构示意图为 ,C的单质与 反应的化学方
反应的化学方
程式为 。
(4)写出A的气态氢化物与B的最高价氧化物对应水化物反应的化学方程式 。
取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol·L-1的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间关系如图所示。
试回答下列问题:
(1)原NaOH溶液的物质的量浓度为 。
(2)曲线A表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是 。
(3)曲线B表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为 mL。
常温下,有A、B、C、D四种电解质分别完全溶于水,所得四种溶液中含有H+、Ba2+、Al3+、Na+、HCO3-、Cl-、OH-、SO42-八种离子(不考虑水解).为检验这四种物质,进行如下实验:
①取少量A的溶液分别与B、C、D反应,依次观察到:白色沉淀和气体、白色沉淀、气体。
②经测定,A和D的溶液显碱性,B和C的溶液pH<7.B与D的溶液反应产生两种沉淀,当D的量增大时,其中一种沉淀不断溶解,最终还存在一种沉淀。
③C与D的溶液反应,无明显现象。经测定,该反应的产物总能量小于反应物总能量。
根据上述实验事实,请回答下列问题:
(1)写出下列物质的化学式:C____________ D______________
(2)A溶液显碱性的原因是(用离子方程式表示)______________________。
(3)A与B在溶液中反应的离子方程式为___________________。
(1)光导纤维的主要成分是_________(填化学式)。碱性溶液不能用带玻璃塞的试剂瓶盛装的原因是(用离子方程式说明)______________。
(2)漂白粉的有效成分是_______________(填物质名称),其漂白原理是(用化学方程式表示)___________。
(Ⅰ)四种短周期元素A、B、C、D的性质或结构信息如下:
①原子半径:A>B>C>D
②四种元素之间形成的某三种分子的比例模型及部分性质如下:
甲: 是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二
是地球上最常见的物质之一,是所有生命体生存的重要资源,约占人体体重的三分之二
乙: 无色,无气味并且易燃.是常见的一种基础能源
无色,无气味并且易燃.是常见的一种基础能源
丙: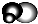 有强氧化性的弱酸,可以用于消毒杀菌
有强氧化性的弱酸,可以用于消毒杀菌
请根据上述信息回答下列问题.
(1)B元素在周期表中的位置第二周期_______________,请写出BC2分子的结构式_____________。
(2)A所在周期中,E元素的单质还原性最强,F元素的某些盐类常用作净水剂.E单质与甲反应有化合物X生成.请写出以下两个反应的离子方程式:
①A元素的单质与物质甲发生的离子反应方程式_____________________。
②F、C两种元素组成的化合物Y可作为高温结构陶瓷材料,X与Y两种化合物在溶液中发生的离子反应方程式为_________________________。
(Ⅱ)某研究小组将CaCl2和H2在一定条件下反应,制得两种化合物(甲和乙).元素组成分析表明化合物甲中钙、氯元素的质量分数分别为52.36%、46.33%;化合物乙的水溶液显酸性.请回答下列问题:
(1)甲的电子式是_________________。
(2)甲与乙溶液反应可得H2,其化学方程式是_____________________。
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的化学方程式是:
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)+49.0kJ
某科学实验将6mol CO2和8mol H2充入一容积为2L的密闭容器中,测得H2的物质的量随时间变化如图中实线所示(图中字母后的数字表示对应的坐标):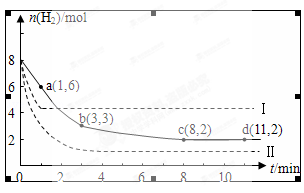
回答下列问题:
(1)由图分析,在下列时间段内反应速率最快的时间段是 (填答案编号)
a.0~1min b.1~3minc.3~8mind.8~11min
(2)该反应在0~8min内CO2的平均反应速率是 mol/(L•min).
(3)仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线所示.与实线相比,曲线Ⅰ改变的条件可能是 ,曲线Ⅱ改变的条件可能是
若实线对应条件下平衡常数为K,曲线Ⅰ对应条件下平衡常数为K1,曲线Ⅱ对应条件下平衡常数为K2,则K、K1和K2的大小关系是
(4)下列表述能表示该反应已达平衡的是 (填答案编号)
a.容器内压强不再改变 b.容器内气体的密度不再改变
c.容器内气体平均摩尔质量不再改变 d.容器内各物质的物质的量相等