高纯六水氯化锶晶体(SrCl2·6H2O)具有很高的经济价值,工业上用难溶于水的碳酸锶(SrCO3)为原料(含少量钡和铁的化合物等),制备高纯六水氯化锶晶体的过程为:
已知: Ⅰ. SrCl2·6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。
Ⅱ.有关氢氧化物开始沉淀和完全沉淀的pH表:
| 氢氧化物 |
Fe(OH)3 |
Fe(OH)2 |
| 开始沉淀的pH |
1.5 |
6.5 |
| 沉淀完全的pH |
3.7 |
9.7 |
(1)操作①加快反应速率的措施有 (写一种)。
碳酸锶与盐酸反应的离子方程式 。
(2)酸性条件下,加入30% H2O2溶液,将Fe2+氧化成Fe3+,其离子方程式为 。
(3)在步骤②-③的过程中,将溶液的pH值由1调节至4时,宜用的试剂为_______。
A.氨水 B.氢氧化锶粉末 C. 氢氧化钠 D.碳酸钠晶体
(4)操作③中所得滤渣的主要成分是 (填化学式)。
(5)步骤④的操作是 、 。
(6)工业上用热风吹干六水氯化锶,适宜的温度是
A.50~60℃ B.70~80℃ C.80~100℃ D.100℃以上
(8分)有下列八种晶体
| A.金刚石 | B.蔗糖 | C.氧化镁 | D.白磷 E.晶体氩 |
F.铝 G.水晶 H 氢氧化钠,用序号回答下列问题:
(1)只有离子键构成的化合物是 。
(2)直接由原子构成的分子晶体是 。
(3)在常温下能导电的是 。
(4)受热熔化时,需克服共价键的化合物是 。
聚芳酯(PAR)是分子主链上带有苯环和酯基的特种工程塑料,在航空航天等领域具有广泛应用。下图是利用乙酰丙酸(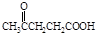 )合成聚芳酯E的路线:
)合成聚芳酯E的路线: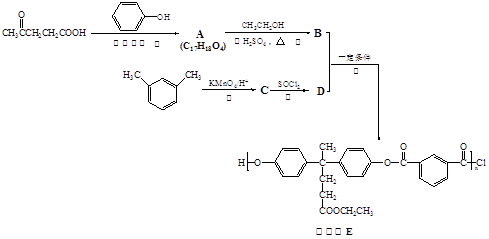
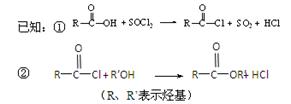
(1)乙酰丙酸中含有的官能团是羰基和(填官能团名称)。
(2)下列关于有机物A的说法正确的是(填字母序号)。
a.能发生加聚反应 b.能与浓溴水反应
c.能发生消去反应 d.能与H2发生加成反应
(3)A→B的化学方程式为。
(4)D的结构简式为。
(5)C的分子式为,符合下列条件的C的同分异构体有种。
①能发生银镜反应②能与NaHCO3溶液反应
③分子中有苯环,无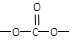 结构④苯环上只有2个取代基
结构④苯环上只有2个取代基
在上述同分异构体中,写出其中任一种与足量NaOH溶液共热反应的化学方程式:。
(10分)近年来,国际原油价格大幅上涨,促使各国政府加大生物能源生产,其中酒精汽油已进入实用化阶段。
(1)乙醇在铜或银作催化剂的条件下,可以被空气中的氧气氧化成X,X可发生银镜反应,请写出X被银氨溶液氧化的反应方程式(标出具体反应条件):
。
(2)乙醇可以与酸性重铬酸钾溶液反应,被直接氧化成Y,Y含有官能团的名称是________。在浓硫酸存在下加热,乙醇与Y反应可生成一种有香味的物质W,化学方程式为。
(3)现有两瓶无色液体,分别盛有Y、W,只用一种试剂就可以鉴别,该试剂可以是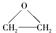
(4)现代石油化工采用银作催化剂,乙烯能被氧气氧化生成环氧乙烷( ),该反应的原子利用率为100%,反应的化学方程式为。
(1)键线式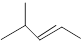 表示的分子式;名称是。
表示的分子式;名称是。
(2)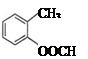 中含有的官能团的名称为。
中含有的官能团的名称为。
与其含有相同官能团,且分子结构中苯环上只有一个取代基的同分异构体有种。
用石油裂化和裂解过程得到的乙烯、丙烯来合成丙烯酸乙酯的路线如下: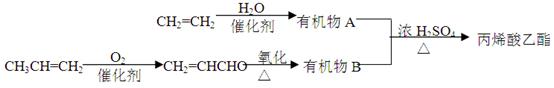
根据以上材料和你所学的化学知识回答下列问题:
(1)丙烯(CH3CH=CH2)中含有的官能团(填名称),A中官能团的电子式__________。
(2)由 CH2=CH2制得有机物A的化学方程式: _______ _,反应类型是 __。
(3)A与B合成丙烯酸乙酯的化学反应方程式是:_____________________________,
反应类型是。
(4)由石油裂解产物乙烯合成聚乙烯塑料的化学方程式是:。