t℃时,在体积不变的容器中发生反应X(g)+3Y(g) 2Z(g)△H<O各组分浓度如下表
2Z(g)△H<O各组分浓度如下表
| 物质 |
X |
Y |
Z |
| 初始浓度/ mol·L-1 |
0.1 |
0.3 |
0 |
| 2min末浓度/mol·L-1 |
0.08 |
|
|
| 平衡浓度/mol·L-1 |
|
|
0.1 |
下列说法不正确的是
A .0~2min的平均速率v(x) ="0." 01 mol·L-1·min-1
B.达平衡时Y的转化率为50%
C.其它条件不变,升高温度,平衡逆向移动
D.其它条件不变,增加X的浓度,ν正增大 逆碱小,平衡正向移动
逆碱小,平衡正向移动
下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是 ()
| A.异戊二烯[ CH2=C(CH3)CH=CH2]与等物质的量的Br2发生加成反应 |
| B.2-氯丁烷(CH3CH2CHClCH3)与NaOH乙醇溶液共热发生消去HCl分子的反应 |
| C.甲苯在一定条件下发生硝化生成一硝基甲苯的反应 |
| D.邻羟基苯甲酸与NaHCO3溶液反应 |
中草药秦皮中含有的七叶树内酯结构是: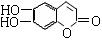 ,(C、H原子未画出,每个折点表示一个C原子)具有抗菌作用,若1 mol 七叶树内酯分别与浓Br2水和NaOH溶液完全反应,则消耗Br2和NaOH的物质的量分别是()
,(C、H原子未画出,每个折点表示一个C原子)具有抗菌作用,若1 mol 七叶树内酯分别与浓Br2水和NaOH溶液完全反应,则消耗Br2和NaOH的物质的量分别是()
A.3,2 B.3,4 C.2,3 D.4,4
除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是()
| 混合物 |
试剂 |
分离方法 |
|
| A |
苯(苯酚) |
溴水 |
过滤 |
| B |
乙烷(乙烯) |
氢气 |
加热 |
| C |
乙酸乙酯(乙酸) |
NaOH溶液 |
蒸馏 |
| D |
淀粉(氯化钠) |
蒸馏水 |
渗析 |
下列各组混合物不能用分液漏斗分离的是()
| A.硝基苯和水 | B.苯和甲苯 | C.四氯化碳和水 | D.溴苯和NaOH溶液 |
某有机物的结构简式为: ,则此有机物可发生的反应类型有:①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化⑦中和()
,则此有机物可发生的反应类型有:①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化⑦中和()
| A.①②③⑤⑥ | B.②③④⑤⑥⑦ | C.①②③④⑤⑥⑦ | D.①②③④⑤⑥ |