现有H2SO4、Ba(OH)2、Na2CO3和氯水四种溶液,有如图所示的相互关系,下图中每条线段两端的物质可以发生化学反应。下列推断合理的是( )。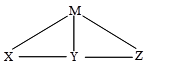
| A.M一定是Ba(OH)2 | B.Y可能是氯水 |
| C.X一定是Na2CO3溶液 | D.Z可能是H2SO4 |
金属及其化合物转化关系是化学学习的重要内容之一。下列各组物质的转化关系中不全部是通过一步反应完成的是()
| A.Na→NaOH→Na2CO3→NaCl |
| B.Al→Al2O3→Al(OH)3→AlCl3 |
| C.Mg→MgCl2→Mg(OH)2→MgSO4 |
| D.Fe→FeCl2→Fe(OH)2→Fe(OH)3 |
氧化还原反应与四种基本类型反应的关系如右图所示,则下列化学反应属于4区的是()。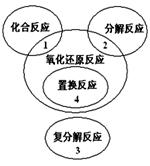
| A.Cl2+2KBr=Br2+2KCl |
| B.2NaHCO3=Na2CO3+H2O+CO2 |
| C.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
| D.2Na2O2+2CO2=2Na2CO3+O2 |
滴加新制氯水后,下列各组离子可能大量存在的是 ( )
| A.Fe3+、Al3+、Cl-、NO3- | B.K+、Na+、I-、SO42- |
| C.Ag+、Ca2+、NH4+、NO3- | D.Na+、Ba2+、CO32-、SO42- |
下列离子方程式书写正确的是()
| A.石灰石与盐酸反应 :CO32-+2H+=CO2↑+H2O |
| B.Cl2通入烧碱溶液中:Cl2+2OH-=Cl-+ClO-+H2O |
| C.氢氧化铜和硫酸反应:OH-+H+=H2O |
| D.将金属铝(无氧化膜)加入氢氧化钠溶液中: Al+ 2OH- = AlO2-+ H2 ↑ |