2013年9月,中国华北华中地区发生了严重的雾霆天气,北京、河北、河南等地的空气污染升为6级空气污染,属于重度污染。汽车尾气、燃煤废气、冬季取暖排放的CO2等都是雾霆形成的原因。
(1)汽车尾气净化的主要原理为; , 在一定温度下,在一体积固定的密闭容器中充入一定量的NO和CO在t1时刻达到平衡状态。
, 在一定温度下,在一体积固定的密闭容器中充入一定量的NO和CO在t1时刻达到平衡状态。
①能判断该反应达到平衡状态的标志是 。
| A.在单位时间内生成1molCO2的同时消耗了lmolCO |
| B.混合气体的密度不再改变 |
| C.混合气体的平均相对分子质量不再改变 |
| D.混合气体的压强不再变化 |
②在t2时刻,将容器的容积迅速扩大到原来的2倍, 在其他条件不变的情况下,t3时刻达到新的平衡状态,之后不再改变条件。请在右图中补充画出从t2 到t4时刻正反应速率随时间的变化曲线: 
(2)改变煤的利用方式可减少环境污染,通常可将水蒸气通过红热的碳得到水煤气,其反应为:
①该反应在 下能自发进行(填“高温”或“低温”)。
②煤气化过程中产生的有害气体H2S可用足量的Na2C03溶液吸收,该反应的离子方程式为 。(已知: ;
; 。
。 ;
;  。)
。)
(3)已知反应: ,现将不同量的CO(g)和H20(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据:
,现将不同量的CO(g)和H20(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下三组数据: 
①实验1条件下平衡常数K= (保留小数点后二位)。
②实验3中,若平衡时,CO的转化率大于水蒸气,则a、b必须满足的关系是 。
③该反应的 0(填“<”或“>”);
0(填“<”或“>”);
矿泉水一般是由岩石风化后被地下水溶解其中可溶部分生成的。此处的风化作用是说矿物与H2O和CO2同时作用的过程。案例如钾长石(KAlSi3O8)风化生成高岭土〔Al2Si2O5(OH)4〕,此反应的离子方程式是:2KAlSi3O8+11H2O+2CO2 2K++2
2K++2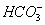 + 4H4SiO4+Al2Si2O5(OH)4,这个反应能发生的原因是_____________。Al2Si2O5(OH)4改写成氧化物的形式为__________________________。
+ 4H4SiO4+Al2Si2O5(OH)4,这个反应能发生的原因是_____________。Al2Si2O5(OH)4改写成氧化物的形式为__________________________。
结构致密的SiO2。二者成分相同,结构不同,化学性质相同,物理性质上表现出差别,具有不同的用途。由石英制取硅胶,经历以下三步,试写出每步反应的化学方程式(是离子反应的,写出离子方程式)。
(1)用NaOH(aq)溶解石英:_________________。
(2)过滤,向滤液中加入盐酸,至沉淀不再产生:_________________。
(3)微热,浓缩硅酸溶液,加热蒸干溶液,并使固体完全分解:_________________。
写出硅胶的一种用途:_________________。
三硅酸镁能被用来治疗胃酸过多的胃溃疡,是因为该物质不溶于水,服用后能中和胃酸,作用持久。把三硅酸镁Mg2Si3O8·nH2O改写成氧化物的形式为________________,它中和胃酸(HCl)的化学方程式是_______ ___________________。
已知Si能与HF(aq)和NaOH(aq)反应:
Si+4HF══SiF4↑+2H2↑
Si+2NaOH+H2O══Na2SiO3+2H2↑
又知硅及其化合物间存在如下图所示的关系:
其中A是制造芯片和光电池的主要原料;B是含硅化合物中的一种气体;某些C可作干燥剂或催化剂的载体;D是一种黏合剂,能将磨砂玻璃黏合在一起;E是一种比H2CO3酸性还弱的酸。
试回答下列问题:
(1)写出A、C、E的化学式:A________、C________、E________。
(2)①~⑦反应中,属于氧化还原反应的是________,属于置换反应的是________,属于离子反应的是________。