在一定温度下,容器内某一反应中两种气态物质M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )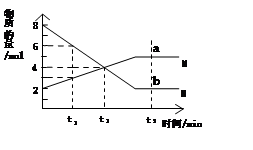
A.反应的化学方程式为:2M N N |
| B.t2时,正逆反应速率相等,反应达到平衡状态 |
| C.t3时,M上a点正反应速率等于N上b点的逆反应速率 |
D.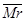 混一定时,N的体积百分含量也一定 混一定时,N的体积百分含量也一定 |
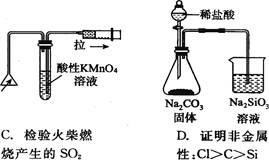
下列实验装置正确且能完成实验目的的是
已知酸性:H2SO4>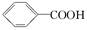 >H2CO3>
>H2CO3>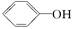 >HCO3—,综合考虑反应物的转化率和原料成本等因素,将
>HCO3—,综合考虑反应物的转化率和原料成本等因素,将 转变为
转变为 的最佳方法是
的最佳方法是
| A.与足量的NaOH溶液共热后,再通入足量CO2 |
| B.与足量的NaOH溶液共热后,再加入适量H2SO4 |
| C.与稀H2SO4共热后,加入足量的NaOH溶液 |
| D.与稀H2SO4共热后,加入足量的Na2CO3溶液 |
近几年科学家发明的一种新型可控电池——锂水电池,工作原理如图所示。下列有关说法不正确的是
| A.碳极发生的反应是:2H2O+2e-=H2↑+2OH- |
| B.有机电解质和水溶液不可以互换区域 |
| C.标况下产生22.4L的氢气时,正极消耗锂的质量为14g |
| D.该装置不仅可提供电能,还可得到清洁的氢气 |
短周期元素W、X、Y、Z在元素周期表中的位置如图所示,其中W的单质是空气的主要成分,化学性质稳定,不易参加化学反应,则下列有关说法中错误的是
| A.W和Y可以形成稳定的化合物,耐热性好,是新型陶瓷材料 |
| B.Z元素的最高价氧化物水化物的酸性强于Y |
| C.四种元素常见的氢化物,一定是Y元素形成的氢化物最不稳定 |
| D.向氢化物WH3与HZ反应后的集气瓶中加入足量的水,所得溶液一定呈酸性 |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.1 molCl2与足量Fe反应转移电子数一定为3NA |
| B.1mol SiO2晶体中含NA个SiO2分子 |
| C.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA |
| D.标准状况下,22.4L氨水含有NA个NH3分子 |